RBSE Solutions for Class 11 Chemistry Chapter 7 साम्यावस्था
Rajasthan Board RBSE Solutions for Class 11 Chemistry Chapter 7 साम्यावस्था Textbook Exercise Questions and Answers.
RBSE Class 11 Chemistry Solutions Chapter 7 साम्यावस्था
RBSE Class 11 Chemistry साम्यावस्था Textbook Questions and Answers
प्रश्न 7.1.
एक द्रव को सीलबंद पात्र में निश्चित ताप पर इसके वाष्प के साथ साम्य में रखा जाता है। पात्र का आयतन अचानक बढ़ा दिया जाता है।
(क) वाष्प - दाब परिवर्तन का प्रारंभिक परिणाम क्या होगा?
(ख) प्रारंभ में वाष्पन एवं संघनन की दर कैसे बदलती है?
(ग) क्या होगा, जब कि साम्य पुनः अंतिम रूप से स्थापित हो जाएगा तब अंतिम वाष्प दाब क्या होगा?
उत्तर:
(क) पात्र का आयतन बढ़ रहा है अतः प्रारम्भ में वाप दाब कम हो जाएगा।
(ख) वाष्पन की दर बढ़ जाएगी क्योंकि आयतन बढ़ने के कारण अधिक स्थान उपलब्ध हो जाएगा लेकिन संघनन की दर कम हो जाएगी।
(ग) साम्य पुनः स्थापित होने पर वाष्पन की दर तथा संघनन की दर समान हो जाएगी तथा अन्त में वही वाष्प दाब स्थापित हो जाएगा क्योंकि निश्चित ताप पर प्रत्येक द्रव का वाष्प दाब निश्चित होता है।

प्रश्न 7.2.
निम्न साम्य के लिए K क्या होगा, यदि साम्य पर प्रत्येक पदार्थ की सांद्रताएँ हैं [SO2] = 0.60M, [O2] = 0.82M एवं [SO3] = 1.90M
2SO2 (g) + O2 (g) → 2SO3 (g)
उत्तर:
अभिक्रिया 2SO2 (g) + O2 (g) → 2SO3 (g) के लिए
\(\mathrm{K}_{\mathrm{c}}=\frac{\left[\mathrm{SO}_3\right]^2}{\left[\mathrm{SO}_2\right]^2\left[\mathrm{O}_2\right]}=\frac{(1.90)^2}{(0.60)^2(0.82)}\)
12.228 (9) = 12.229mol L-1
Kc = 12.229mol L-1
प्रश्न 7.3.
एक निश्चित ताप एवं कुल दाब 105 Pa पर आयोडीन वाष्प में आयतनानुसार 40% आयोडीन परमाणु होते हैं।
I2(g) = 2I(g) साम्य के लिए Kp की गणना कीजिए।
उत्तर:
I2 तथा I के मोल आयतन के समानुपाती होते हैं।
प्रश्नानुसार I2 तथा I का अनुपात 60 : 40 (3 : 2)
कुल मोल = (3 + 2) = 5
I2 का आंशिक दाब = 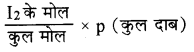
= 3/5 × 105 Pa = 6 × 104 Pa
इसी प्रकार [I] का आंशिक दाब = 2/5 × 105 Pa
= 4 x 104 Pa
अभिक्रिया I2(g) → 2I(g) के लिए
\(\mathrm{K}_{\mathrm{p}}=\frac{\left(\mathrm{p}_{\mathrm{l}}\right)^2}{\mathrm{p}_{\mathrm{l}_2}}=\frac{\left(4 \times 10^4\right)^2}{6 \times 10^4}\)
K = 2.67 x 104
= 2.666 × 104
kP = 2.67 × 104
प्रश्न 7.4.
निम्नलिखित में से प्रत्येक अभिक्रिया के लिए साम्य स्थिरांक K का व्यंजक लिखिए:
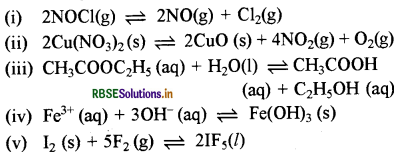
उत्तर:

प्रश्न 7.5.
Kp के मान से निम्नलिखित में से प्रत्येक साम्य के लिए Kc का मान ज्ञात कीजिए:
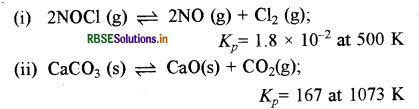
उत्तर:
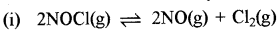
∆n(g) = 3 - 2 = 1 Kp = 1.8 x 102 atm
R = 0.0821
Latm k-1 mol-1 T = 500 k
Kp = Kc (RT)∆n
Kc = Kp/(RT)∆n
\(=\frac{1.8 \times 10^{-2} \mathrm{~atm}}{\left(0.0821 \mathrm{~L} \mathrm{~atm}^{-1} \mathrm{~mol}^{-1} \times 500 \mathrm{k}^1\right)}\)
= 4.384 × 10-4
Kc = 4.38 × 10-4
(ii) 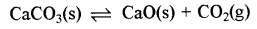
∆nn(g) = 1 - 0 = 1 kp = 167 atm.
R = 0.0821 L atm k-1 mol-1 T= 1073 k
Kp = Kc(RT)∆n
\(=\frac{167 \mathrm{~atm}}{\left(0.0821 \mathrm{~L} \mathrm{~atm} \mathrm{\textrm {k } ^ { - 1 } \mathrm { mol } ^ { - 1 } \times 1 0 7 3 \mathrm { k } ) ^ { 1 }}\right.}\)
Kc = 1.89 = 1.90
प्रश्न 7.6.
साम्य 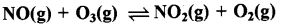 के लिए 1000K पर Kc = 6.3 x 1014 है। साम्य में अग्र एवं प्रतीप दोनों अभिक्रियाएँ प्राथमिक रूप से द्विअणुक हैं। प्रतीप अभिक्रिया के लिए Kc क्या है?
के लिए 1000K पर Kc = 6.3 x 1014 है। साम्य में अग्र एवं प्रतीप दोनों अभिक्रियाएँ प्राथमिक रूप से द्विअणुक हैं। प्रतीप अभिक्रिया के लिए Kc क्या है?
उत्तर:
प्रतीप अभिक्रिया के लिए साम्य स्थिरांक:
\(\mathrm{K}_{\mathrm{c}}^1=\frac{1}{\mathrm{~K}_{\mathrm{c}}}=\frac{1}{6.3 \times 10^{14}}\) = 1.59 x 10-15 KC = 1.59 x 10-15

प्रश्न 7.7.
साम्य स्थिरांक का व्यंजक लिखते समय समझाइए कि शुद्ध द्रवों एवं ठोसों को उपेक्षित क्यों किया जा सकता है?
उत्तर:
शुद्ध द्रव या शुद्ध ठोस के लिए

स्थिर ताप पर शुद्ध द्रव या शुद्ध ठोस का घनत्व तथा मोलर द्रव्यमान स्थिर रहता है। अतः मोलर सान्द्रता भी स्थिर होगी तथा यह पदार्थ की मात्रा पर निर्भर नहीं करती। अतः साम्य स्थिरांक व्यंजक लिखते समय शुद्ध द्रवों एवं शुद्ध ठोसों को उपेक्षित कर दिया जाता है।
प्रश्न 7.8.
N2 एवं O2 के मध्य निम्नलिखित अभिक्रिया होती है:
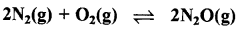
यदि एक 10L के पात्र में 0.482 मोल N2 एवं 0.933 मोल O2 रखे जाएँ तथा एक ताप, जिस पर N2O बनने दिया जाए तो साम्य मिश्रण का संघटन ज्ञात कीजिए Kc = 2.0 × 10-37
उत्तर:
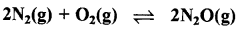
|
प्रारम्भ में मोल |
0.482 |
0.933 |
0 |
|
साम्य पर मोल |
0.482 - x |
0.933 - x |
x |
(माना साम्य पर N2 के x मोल साम्य पर वियोजित होते हैं)
Kc का मान बहुत कम (2 x 10-37) है अर्थात् साम्य पर अभिकारकों की सान्द्रता बहुत अधिक है। अतः x का मान बहुत कम होगा, जिसे अन्य मान की तुलना में नगण्य मान सकते हैं।

Kc = 2.0 × 10-37
अतः
2.0 × 10-37 = \(\frac{(0.1 x)^2}{(0.0482)^2(0.0933)}\)
x = 6.58 × 10-20
x = 6.6 x 10-20
अतः
[N2O] = 0.1 x x = 0.1 × 6.6 × 10-20
= 6.6 × 10-21 mol L-1
प्रश्न 7.9.
निम्नलिखित अभिक्रिया के अनुसार नाइट्रिक ऑक्साइड Br2 से अभिक्रिया कर नाइट्रोसिल ब्रोमाइड बनाती है:
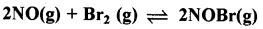
जब स्थिर ताप पर एक बंद पात्र में 0.087 मोल NO एवं 0.0437 मोल Br: मिश्रित किए जाते हैं, तब 0.0518 मोल NOBr प्राप्त होती है। NO एवं Br2 की साम्य मात्रा ज्ञात कीजिए।
उत्तर:
2NO(g) + Br2(g) → 2NOBr(g)
अभिक्रिया की रससमीकरणमिति के अनुसार 2 मोल NO, 1 मोल Bra से क्रिया कर 2 मोल NOBr बनाता है। अतः
2NO(g) + Br2(g) → 2NOBr(g)
|
प्रारम्भ में मोल |
0.087 |
0.437 |
0 |
|
साम्य पर मोल |
0.087 - x |
0.437 – x/2 |
x |
(चूँकि x= 0.0518 दिया गया है)
अतः साम्य पर [NO] = 0.087 - 0.0518 = 0.0352 mol
[Br2] = 0.0437 - \(\frac{0.0518}{2}\) = 0.0178 mol
प्रश्न 7.10.
साम्य 2SO2 (g) + O2(g) → 2SO3(g) लिए 450K पर Kp = 2.0 x 1010 bar है। इस ताप पर Kc का मान ज्ञात कीजिए।
उत्तर:
प्रश्न में दी गई अभिक्रिया के लिए
∆n(g) = 2 - 3 = -1
Kp = Kc (RT)∆n
\(\mathrm{K}_{\mathrm{o}}=\frac{\mathrm{K}_{\mathrm{p}}}{(\mathrm{RT})^{\Delta \mathrm{n}}}=\frac{2.0 \times 10^{10} \mathrm{bar}}{\left(0.0831 \mathrm{~L} \mathrm{bar} \mathrm{k}^{-1} \mathrm{~mol}^{-1} \text { bar } \times 450 \mathrm{k}\right)^{-1}}\)
Kp = 2 × 1010 (0.0831 × 450 )
Kc = 7.47 × 101 Lmol-1
Kc = 7.47 × 10 m-1
प्रश्न 7.11.
HI (g) का एक नमूना 0.2 atm दाब पर एक फ्लास्क में रखा जाता है। साम्य पर HI (g) का आंशिक दाब 0.04 atm है। यहाँ दिए गए साम्य के लिए K का मान क्या होगा?
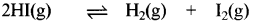
उत्तर:
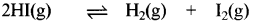
माना साम्य पर x मोल HI का वियोजन हो जाता है।
साम्य पर दाब 0.2 x
अतः
x = 0.16, X/2 = 0.08
\(\mathrm{K}_{\mathrm{p}}=\frac{\mathrm{p}_{\mathrm{H}_2} \times \mathbf{p}_{\mathrm{i}_2}}{\left(\mathrm{p}_{\mathrm{H} \mathrm{I}}\right)^2}=\frac{\frac{\mathrm{x}}{2} \times \frac{\mathrm{x}}{2}}{(0.2-\mathrm{x})^2}\)
प्रश्नानुसार (0.2 - x = 0.04)
\(\mathrm{K}_{\mathrm{p}}=\frac{0.08 \times 0.08}{(.04)^2}\)
Kp = 4.0
प्रश्न 7.12.
500K ताप पर एक 20L पात्र में N2 के 1.57 मोल H2 के 1.92 मोल एवं NH3 के 8.13 मोल का मिश्रण लिया जाता है। अभिक्रिया 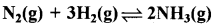 के लिए K का मान 1.7 x 102 है। क्या अभिक्रिया - मिश्रण साम्य में है? यदि नहीं, तो नेट अभिक्रिया की दिशा क्या होगी?
के लिए K का मान 1.7 x 102 है। क्या अभिक्रिया - मिश्रण साम्य में है? यदि नहीं, तो नेट अभिक्रिया की दिशा क्या होगी?
उत्तर:

Qc = 2.379 × 10 Kc = 1.7 x 102 ( दिया गया है।)
चूँकि Qc = Kc अतः साम्यावस्था नहीं है।
Qc > Kc अतः अभिक्रिया प्रतीप दिशा में होगी।

प्रश्न 7.13.
एक गैसीय अभिक्रिया के लिए
\(K_{\mathrm{c}}=\frac{\left[\mathrm{NH}_3\right]^4\left[\mathrm{O}_2\right]}{\left[\mathrm{NO}^*\left[\mathrm{H}_2 \mathrm{O}\right]\right.}\) है, तो
इस व्यंजक के लिए संतुलित रासायनिक समीकरण लिखिए।
उत्तर:
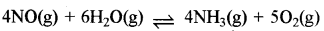
प्रश्न 7.14.
H2O का एक मोल एवं CO का एक मोल 725 K ताप पर 10L के पात्र में लिए जाते हैं। साम्य पर 40% जल ( भारात्मक) CO के साथ निम्नलिखित समीकरण के अनुसार अभिक्रिया करता है:
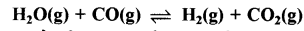
अभिक्रिया के लिए साम्य स्थिरांक की गणना कीजिए।
उत्तर:
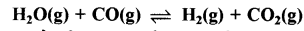
|
प्रारम्भ में मोल |
1 |
1 |
0 |
0 |
|
साम्य पर मोल |
1 - 4 |
1 - 4 |
4 |
4 |
( साम्य पर 40% (0.4) जल अभिक्रिया कर रहा है। )
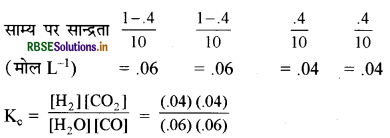
Kc = 0.44
प्रश्न 7.15.
700K ताप पर अभिक्रिया imm के लिए साम्य स्थिरांक 54.8 है। यदि हमने शुरू में HI (g) लिया हो तथा 700K ताप पर साम्य स्थापित हो, तथा साम्य पर 0.5mol L - HI (g) उपस्थित हो, तो साम्य पर H2(g) एवं I2(g) की सांद्रताएँ क्या होंगी?
उत्तर:
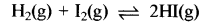
माना साम्य पर H2 तथा I2 दोनों के मोल = x
\(\mathrm{K}_{\mathrm{o}}=\frac{[\mathrm{HI}]^2}{\left[\mathrm{H}_2\right]\left[\mathrm{I}_2\right]}=\frac{(0.5)^2}{(\mathrm{x})(\mathrm{x})}\)
x = 0.06754 = 0.068
अतः साम्य पर [H2] = 0.068mol L-1
[I2] = 0.068mol L-1
प्रश्न 7.16.
ICI, जिसकी सांद्रता प्रारम्भ में 0.78M है, को यदि साम्य पर आने दिया जाए, तो प्रत्येक की साम्य पर सांवताएँ क्या होंगी?
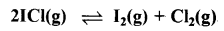
Kc = 0.14
उत्तर:
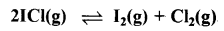
|
प्रारम्भ में मोल |
0.78 M |
0 |
0 |
|
साम्य पर मोल |
0.78 – 2x |
x |
x |
(माना साम्य पर ICI के 2x मोल क्रिया करते हैं।)
\(\mathrm{K}_{\mathrm{c}}=\frac{\left[\mathrm{I}_2\right]\left[\mathrm{Cl}_2\right]}{\left[\mathrm{ICl}_2\right]^2}\)
\(\begin{aligned} & 0.14=\frac{(\mathrm{x})(\mathrm{x})}{(0.78-2 x)^2} \\ & \sqrt{0.14}=\frac{\mathrm{x}}{(0.78-2 \mathrm{x})} \\ & 0.374=\frac{\mathrm{x}}{0.78-2 \mathrm{x}} \end{aligned}\)
x = 0.2917 - 0.748x
x + 0.748x = 0.2917
x (1 + 0.748) = 0.2917
\(\mathrm{x}=\frac{0.2917}{1.748}\)
x = 0.1668 = 1.167 M
अतः साम्य पर [I2] = [Cl2] = 0.167 M
[ICI] = 0.78 - 2 x 0.167 = 0.446M.
प्रश्न 7.17.
नीचे दर्शाए गए साम्य में 899 K पर Kp का मान 0.04 atm है। C2H6 की साम्य पर सांद्रता क्या होगी यदि 4.0 atm दाब पर C2H6 को एक फ्लास्क में रखा गया है एवं साम्यावस्था पर आने दिया जाता है?
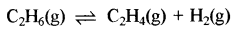
उत्तर:
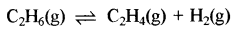
|
प्रारम्भ में दाब |
4.0 atm |
0 |
0 |
|
साम्य पर दाब |
4 - p |
p |
p |
p2 = 0.04 (4 - p)
p2 = 0.16 - 0.04p
p2 +0.04p - 0.16 = 0
p = 0.38
\(\mathrm{p}=\frac{(-0.04) \pm \sqrt{0.0016-4(-0.16)}}{2}\)
= (-0.04) + 0.8/2 = 0.76/2 = 0.38
अतः साम्य पर [C2H6] = 40.38 = 3.62atm.
प्रश्न 7.18.
एथेनॉल एवं ऐसीटिक अम्ल की अभिक्रिया से एथिल ऐसीटेट बनाया जाता है एवं साम्य को इस प्रकार दर्शाया जा सकता है:
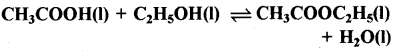
(i) इस अभिक्रिया के लिए सांद्रता अनुपात (अभिक्रिया- भागफल) Qc लिखिए (टिप्पणी यहाँ पर जल आधिक्य में नहीं है एवं विलायक भी नहीं है)
(ii) यदि 293K पर 1.0 मोल ऐसीटिक अम्ल एवं 0.18 मोल एथेनॉल प्रारंभ में लिये जाएं तो अंतिम साम्य मिश्रण में 0.171 मोल एथिल ऐसीटेट है। साम्य स्थिरांक की गणना कीजिए।
(iii) 0.5 मोल एथेनॉल एवं 1.0 मोल ऐसीटिक अम्ल से प्रारंभ करते हुए 293K ताप पर कुछ समय पश्चात् एथिल ऐसीटेट के 0.214 मोल पाए गए तो क्या साम्य स्थापित हो गया?
उत्तर:
(i) Qc (सान्द्रता अनुपात)
\(=\frac{\left[\mathrm{CH}_3 \mathrm{COOC}_2 \mathrm{H}_5\right]\left[\mathrm{H}_2 \mathrm{O}\right]}{\left[\mathrm{CH}_3 \mathrm{COOH}\right]\left[\mathrm{C}_2 \mathrm{H}_5 \mathrm{OH}\right]}\)

Kc = 3.919 = 3.92
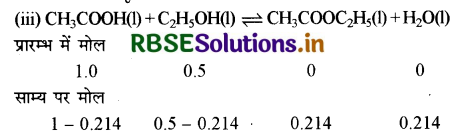
\(Q_c=\frac{0.214 \times 0.214}{0.786 \times 0.286}\)
= 0.2037 = 0.204
Qc < Kc अतः साम्यावस्था स्थापित नहीं होगी।
प्रश्न 7.19
437K ताप पर निर्वात में PCl5 का एक नमूना एक फ्लास्क में लिया गया। साम्य स्थापित होने पर PCl5 की सांद्रता 0.5 x 10-1 mol L-1 पाई गई, यदि K. का मान 8.3 x 10-3 है, तो साम्य पर PCl3 एवं Cl2 की सांद्रताएं क्या होंगी?
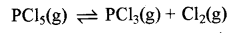
उत्तर:
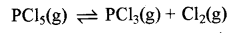
x 2 = 8.3 × 10-3 x 0.05
x = 2 × 10-2 = 0.02
[PCl3] = x = 0.02M, [Cl2] = x = 0.02 M
0.02 mol L-1

प्रश्न 7.20.
लौह-अयस्क से स्टील बनाते समय जो अभिक्रिया होती है, वह आयरन (II) ऑक्साइड का कार्बन मोनोऑक्साइड के द्वारा अपचयन है एवं इससे धात्विक लौह एवं CO2 मिलते हैं।
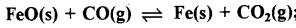
Kp = 0.265 atm 1050K पर 1050K पर CO एवं CO2 के साम्य पर आंशिक दाब क्या होंगे, यदि उनके प्रारंभिक आशिक दाब निम्न हैं:
PCO = 1.4 atm एवं PCO2 = 0.80 atm
उत्तर:
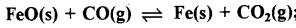
प्रारम्भिक दाब - 1.4 atm.
\(\mathrm{Q}_{\mathrm{p}}=\frac{\mathrm{p}_{\mathrm{CO}_2}}{\mathrm{p}_{\mathrm{CO}}}=\frac{0.80}{1.4}=0.571\)
Kp = 0.265 atm; चूँकि Qp > Kp अतः अभिक्रिया प्रतीप दिशा में होगी।
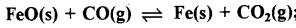
माना साम्य पर CO2 का patm क्रिया करता है।
साम्य पर दाब:
(1.4 + p) (0.80 - p)
\(\mathrm{K}_{\mathrm{p}}=\frac{\mathrm{p}_{\mathrm{CO}_2}}{\mathrm{p}_{\mathrm{CO}}}, 0.265=\frac{0.80-\mathrm{p}}{1.4+\mathrm{p}}\)
= 0.80 - p 0.371 +0.265p
= 0.8 - p
1.265p = 0.8 - 0.371
\(\mathrm{p}=\frac{0.429}{1.265}\)
p= 0.339
अतः साम्य पर Pco = 14 + p = 1.4 + 0.339
= 1.739 atm
PCO2 = 0.80 - p = 0.80 - 0.339
PCO2 = 0.461 atm.
प्रश्न 7.21.
अभिक्रिया N2 (g) + 3H2 (g) → 2NH3 (g) के लिए (500K) पर साम्य स्थिरांक K 0.061 है। एक विशेष समय पर मिश्रण का संघटन इस प्रकार है:
3.0mol L-1 N2, 2.0mol L-1 H2 एवं 0.5mol L-1
NH3 क्या अभिक्रिया साम्य में है? यदि नहीं तो साम्य स्थापित करने के लिए अभिक्रिया किस दिशा में अग्रसर होगी?
उत्तर:
N2 (g) + 3H2 (g) → 2NH3 (g)
किसी समय पर सान्द्रता mol L-1 3.0 2.0 0.50
अतः
\(\mathrm{Q}_{\mathrm{c}}=\frac{\left[\mathrm{NH}_3\right]^2}{\left[\mathrm{~N}_2\right]\left[\mathrm{H}_2\right]^3}=\frac{(0.50)^2}{(3.0)(2.0)^3}\)
= 0.0104
Kc = 0.061 Qc तथा Kc बराबर नहीं हैं। अतः इस समय पर साम्य स्थापित नहीं होगा तथा Qc < Kc अतः साम्य स्थापित करने के लिए अभिक्रिया अग्र दिशा में जाएगी तथा अधिक उत्पाद बनेंगे।
प्रश्न 7.22.
ब्रोमीन मोनोक्लोराइड (BrCI) विघटित होकर ब्रोमीन एवं क्लोरीन देता है तथा साम्य स्थापित होता है:
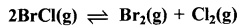
इसके लिए 500K पर Kc = 32 है। की सांद्रता 3.3 x 10-3 mol L-1 इसकी सांद्रता क्या होगी?
उत्तर:
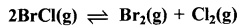
(माना साम्य पर BrCI के x मोल क्रिया करते हैं।)
\(\mathrm{K}_{\mathrm{c}}=\frac{\left[\mathrm{Br}_2\right]\left[\mathrm{Cl}_2\right]}{\left[\mathrm{BrCl}^2\right.}, 32=\frac{(\mathrm{x} / 2)(\mathrm{x} / 2)}{\left[\left(3.30 \times 10^{-3}\right)-\mathrm{x}\right]^2}\)
दोनों पक्षों का वर्गमूल लेने पर
\(5.66=\frac{x / 2}{(0.0033-x)}\)
5.66 (0.0033 - x) = 0.5x
0.0186 - 5.66x = 0.5x
6.16x = 0.0186
x = 0.0030
x = 3.0 × 10-3
अतः साम्य पर [BrCl] की सान्द्रता (3.30 x 103 - x)
= 3.30 × 10-3 - 3.0 × 10-3
[BrCl] = 0.30 × 10-3
= 3.0 × 10-4 mol L-1
प्रश्न 7.23.
1127K एवं 1 atm दाब पर CO तथा CO2 के गैसीय मिश्रण जो कि ठोस कार्बन के साथ साम्यावस्था में है, में 90.55% ( भारात्मक) CO है।
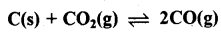
उपरोक्त ताप पर अभिक्रिया के लिए K के मान की गणना कीजिए।
उत्तर:
माना CO तथा CO2 का कुल द्रव्यमान = 100g
CO = 90.55% (भारात्मक) साम्य पर अतः CO का द्रव्यमान
= 90.55g तथा CO2 का द्रव्यमान = 100 - 90.55 = 9.45g
अतः CO के मोल = 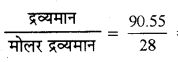 = 90.55/28 = 3.233
= 90.55/28 = 3.233
CO2 के मोल = 9.45/44 = 0.214
मिश्रण में CO का आंशिक दाब = PCO = \(\frac{3.233}{3.233+0.214}\)
1 atm = 0.93atm.
PCO2 = \(\frac{0.214}{0.214+3.233}\) × 1 atm = 0.062 atm.
\(\mathrm{K}_{\mathrm{p}}=\frac{\mathrm{p}_{\mathrm{CO}}^2}{\mathrm{p}_{\mathrm{CO}_2}}=\frac{(0.93)^2}{(0.062)}\)
= 1.35
∆ng = 2 - 1 = 1
\(\mathrm{K}_{\mathrm{c}}=\frac{\mathrm{K}_{\mathrm{p}}}{(\mathrm{RT})^{\Delta \mathrm{n}}}=\frac{13.95}{0.0821 \times 1127}\)
= 0.150
प्रश्न 7.24.
298K पर NO एवं O2 से NO2 बनती है:
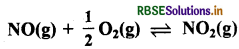
अभिक्रिया के लिए (क) ∆G° एवं (ख) साम्य स्थिरांक की गणना कीजिए:
∆fG° (NO2) = 52.0kJ/mol
∆fG° (NO) = 87.0kJ/mol
∆rG° (O2) = 0kJ/mol
उत्तर:
(क) ∆fG° = ∑∆fG° (उत्पाद) - ∑∆fG° (अभिकारक)
= ∆fG° (NO2) - [∆fG° (NO) + 1/2∆fG°(O2)]
= 52.0 - (87.0 + 1/2 × 0)
= - 35.0kJ mol L-1
(ख) -∆G° = 2.303RT log K
(-35000) = 2.303 x 8.314 x 298 log K
log K = 6.1341
K = Antilog 6.1341 = 1.361 × 106

प्रश्न 7.25.
निम्नलिखित में से प्रत्येक साम्य में जब आयतन बढ़ाकर दाब कम किया जाता है, तब बतलाइए कि अभिक्रिया के उत्पादों के मोलों की संख्या बढ़ती है या घटती है या समान रहती है?
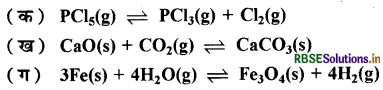
उत्तर:
साम्य पर ला - शातेलिए के सिद्धान्त के अनुसार (क) दाब कम होने से अग्र अभिक्रिया का वेग बढ़ेगा अतः उत्पादों के मोलों की संख्या बढ़ती है। (ख) दाब कम होने से पश्च अभिक्रिया का वेग बढ़ेगा अतः उत्पादों के मोलों की संख्या घटती है। (ग) इस अभिक्रिया पर दाब का कोई प्रभाव नहीं होगा अतः उत्पाद के मोलों की संख्या समान रहती है (∆n(g) = 0)
प्रश्न 7.26.
निम्नलिखित में से दाब बढ़ाने पर कौन-कौनसी अभिक्रियाएँ प्रभावित होंगी? यह भी बताएँ कि दाब परिवर्तन करने पर अभिक्रिया अग्र या प्रतीप दिशा में गतिमान होगी?
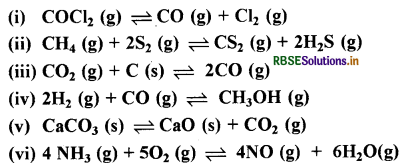
उत्तर:
अभिक्रियाएँ जिनमें ∆n(g) = 0 नहीं है अर्थात् गैसीय उत्पादों तथा गैसीय अभिकारकों के मोलों की संख्या समान नहीं है। उनमें दाब बढ़ाने पर अभिक्रियाएँ प्रभावित होंगी अतः अभिक्रिया (i), (iii), (iv), (v) तथा (vi) प्रभावित होगी। ला शातेलिए के सिद्धान्त के अनुसार साम्य पर दाब बढ़ाने से अभिक्रिया उस दिशा में जाती है जिधर गैसीय पदार्थ कम हो ।
(i) ∆n(g) = +1 अतः अभिक्रिया प्रतीप दिशा में गतिमान होगी।
(ii) ∆n(g) = 0 अभिक्रिया पर दाब का कोई प्रभाव नहीं होगा।
(iii) ∆n = + 1 अभिक्रिया प्रतीप दिशा में गतिमान होगी।
(iv) ∆n = - 2 अभिक्रिया अग्र दिशा में गतिमान होगी।
(v) ∆n = + अभिक्रिया प्रतीप दिशा में गतिमान होगी।
(vi) ∆n = + 1 अभिक्रिया प्रतीप दिशा में गतिमान होगी।
प्रश्न 7.27.
निम्नलिखित अभिक्रिया के लिए 1024K पर साम्य स्थिरांक 1.6 x 105 है।
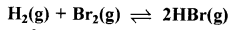
यदि HBr के 10.0bar सीलयुक्त पात्र में डाले जाएँ, तो सभी गैसों के 1024K पर साम्य दाब ज्ञात कीजिए।
उत्तर:
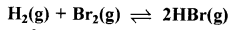
|
प्रारम्भिक दाब |
0 |
0 |
10.0 bar |
|
साम्य पर दाब |
p/2 |
p/2 |
(10 – p) |
चूँकि प्रारम्भ में उत्पाद लिया गया है अतः अभिक्रिया पश्च दिशा में हो रही है तथा माना HBr के p bar साम्य पर क्रिया करते हैं।
\(\begin{aligned} & \mathrm{K}_{\mathrm{p}}=\frac{\mathrm{p}_{\mathrm{HBr}}^2}{\mathrm{p}_{\mathrm{H}_2} \times \mathrm{p}_{\mathrm{Br}_2}} \\ & 1.6 \times 10^5=\frac{10-\mathrm{p}}{\mathrm{p} / 2 \times \mathrm{p} / 2} \end{aligned}\)
दोनों पक्षों का वर्गमूल लेने पर
\(4 \times 10^2=\frac{10-\mathrm{p}}{\mathrm{p} / 2}\)
200 p = 10-p
p = 10/201 bar
PH2 = p/2 = 1/2(10/201) bar = 2.5 x 10-2 bar
PBr2 = p/2 = 2.5 x 10-2 bar
PHBr = 10 - p 10 bar (क्योंकि p <<< 10)
प्रश्न 7.28.
निम्नलिखित ऊष्माशोषी अभिक्रिया के अनुसार ऑक्सीकरण द्वारा डाइहाइड्रोजन गैस प्राकृतिक गैस से प्राप्त की जाती है:
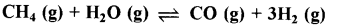
(क) उपर्युक्त अभिक्रिया के लिए K, का व्यंजक लिखिए।
(ख) K एवं अभिक्रिया मिश्रण का साम्य पर संघटन किस प्रकार प्रभावित होगा, यदि
(i) दाब बढ़ा दिया जाए
(ii) ताप बढ़ा दिया जाए
(iii) उत्प्रेरक प्रयुक्त किया जाए।
उत्तर:
\(\text { (क) } \mathbf{K}_{\mathrm{p}}=\frac{\mathbf{p}_{\mathrm{CO}} \times\left(\mathbf{p}_{\mathrm{H}_2}\right)^3}{\mathbf{p}_{\mathrm{CH}_4} \times \mathbf{p}_{\mathrm{H}_2 \mathrm{O}}}\)
(ख) (i) ला शातलिए के सिद्धान्त के अनुसार दाब बढ़ाने पर साम्य प्रतीप दिशा में जाएगा [गैसीय अणुओं (मोलों) की संख्या कम] लेकिन Kp पर कोई प्रभाव नहीं होगा तथा साम्य संघटन भी अप्रभावित रहेगा।
(ii) यह ऊष्माशोषी अभिक्रिया है अतः ताप बढ़ाने पर अभिक्रिया अग्र दिशा में अग्रसर होगी तथा Kg का मान बढ़ेगा। अतः साम्य संघटन भी प्रभावित होगा तथा उत्पादों की सान्द्रता अधिक होगी।
(iii) उत्प्रेरक से K अप्रभावित रहेगा तथा साम्य संघटन भी समान रहेगा लेकिन उत्प्रेरक की उपस्थिति में साम्य शीघ्र स्थापित हो जाएगा।
प्रश्न 7.29
साम्य 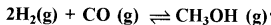 पर प्रभाव बताइए:
पर प्रभाव बताइए:
(क) H2 मिलाने पर
(ख) CH3OH मिलाने पर
(ग) CO हटाने पर
(घ) CH3OH हटाने पर।
उत्तर:
(क) H2 मिलाने पर साम्य अग्र दिशा में जाएगा
(ख) CH3OH मिलाने पर साम्य प्रतीप दिशा में जाएगा
(ग) CO हटाने पर भी साम्य प्रतीप दिशा में जाएगा
(घ) CH3OH हटाने पर साम्य अग्र दिशा में जाएगा।
प्रश्न 7.30
473K पर फॉस्फोरस पेंटाक्लोराइड (PCl5) के विघटन के लिए K का मान 8.3 ×10 है। यदि विघटन इस प्रकार दर्शाया जाए। 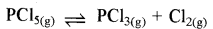 ∆H° = 124.0kJ mol (क) अभिक्रिया के लिए K का व्यंजक लिखिए। (ख) प्रतीप अभिक्रिया के लिए समान ताप पर K का मान क्या होगा? (ग) यदि (i) और अधिक PCl5 मिलाया जाए, (ii) दाब बढ़ाया जाए तथा (iii) ताप बढ़ाया जाए, तो Kc पर क्या प्रभाव होगा?
∆H° = 124.0kJ mol (क) अभिक्रिया के लिए K का व्यंजक लिखिए। (ख) प्रतीप अभिक्रिया के लिए समान ताप पर K का मान क्या होगा? (ग) यदि (i) और अधिक PCl5 मिलाया जाए, (ii) दाब बढ़ाया जाए तथा (iii) ताप बढ़ाया जाए, तो Kc पर क्या प्रभाव होगा?
उत्तर:
(क) अभिक्रिया 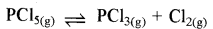
\(\mathrm{K}_{\mathrm{c}}=\frac{\left[\mathrm{PCl}_3\right]\left[\mathrm{Cl}_2\right]}{\left[\mathrm{PCl}_5\right]}\)
= 8.3 x 10-3
(ख) प्रतीप अभिक्रिया के लिए Kc

Kc = 120.48
(i) और अधिक PCl5 मिलाने पर Kc का मान अपरिवर्तित
(ii) दाब बढ़ाने पर Kc का मान अप्रभावित रहेगा।
(iii) इस अभिक्रिया के लिए ∆rH° = +ve, (ऊष्माशोषीं अभिक्रिया) अतः इसमें ताप बढ़ाने पर साम्य अग्र दिशा में जाएगा तथा Kc का मान बढ़ेगा।
प्रश्न 7.31.
हाबर विधि में प्रयुक्त हाइड्रोजन को प्राकृतिक गैस से प्राप्त मेथेन को उच्च ताप की भाप से क्रिया कर बनाया जाता है। दो पदों वाली अभिक्रिया में प्रथम पद में CO एवं H2 बनती हैं। दूसरे पद में प्रथम पद में बनने वाली CO और अधिक भाप से अभिक्रिया करती है।
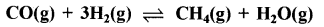
यदि 400°C पर अभिक्रिया पात्र में सममोलर मिश्रण इस प्रकार लिया जाए कि pCO = pH2O = 4.0bar, H2 का साम्यावस्था पर आंशिक दाब क्या होगा? 400°C पर Kp = 10.1
उत्तर:
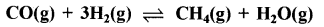
(माना साम्यावस्था पर H2 का आंशिक दाब =p बार )
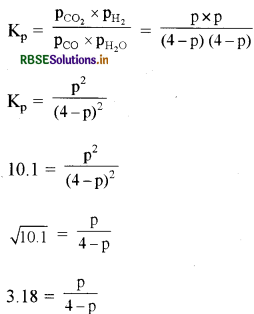
P = 3.04 bar
अतः
PH2 = 3.04 bar
प्रश्न 7.32.
बताइए कि निम्नलिखित में से किस अभिक्रिया में अभिकारकों एवं उत्पादों की सांद्रता सुप्रेक्ष्य (appreciable) होगी (अर्थात् तुलनात्मक मात्रा में होगी):
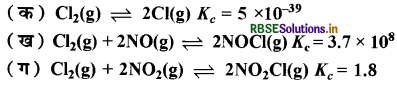
उत्तर:
अभिक्रिया (ग) में Kc का मान न तो बहुत अधिक है तथा न ही बहुत कम है, अतः इसमें साम्य पर अभिकारकों एवं उत्पादों की सान्द्रता तुलनात्मक मात्रा में होगी अर्थात् सुप्रेक्ष्य होगी। अभिक्रिया (क) में Kc बहुत कम तथा (ख) में Kc का मान बहुत अधिक है।
प्रश्न 7.33.
25°C पर अभिक्रिया 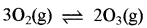 के लिए Kc का मान 2.0 × 10-50 है। यदि वायु में 25°C ताप पर O2 की साम्यावस्था सांद्रता 1.6 ×10-2 है, तो 0, की सांद्रता क्या होगी?
के लिए Kc का मान 2.0 × 10-50 है। यदि वायु में 25°C ताप पर O2 की साम्यावस्था सांद्रता 1.6 ×10-2 है, तो 0, की सांद्रता क्या होगी?
उत्तर:
अभिक्रिया 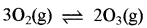
के लिए
Kc = 2.0 × 10-50, [O2] = 1.6 × 10-2
\(\mathrm{K}_{\mathrm{c}}=\frac{\left[\mathrm{O}_3\right]^2}{\left[\mathrm{O}_2\right]^3}, 2.0 \times 10^{-50}=\frac{\left[\mathrm{O}_3\right]^2}{\left(1.6 \times 10^{-2}\right)^3}\)
[O3]2 = (2.0 × 10-50) × (1.6 × 10-2)3
[O3] = 2.86 × 10-28 M

प्रश्न 7.34.
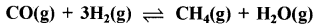 अभिक्रिया एक लिटर फ्लास्क में 1300K पर साम्यावस्था में है। इसमें CO के 0.3 मोल, H2 के 0.1 मोल H2O के 0.02 मोल एवं CH4 की अज्ञात मात्रा हैं। दिए गए ताप पर अभिक्रिया के लिए Kc का मान 3.90 है। मिश्रण में CH4 की मात्रा ज्ञात कीजिए।
अभिक्रिया एक लिटर फ्लास्क में 1300K पर साम्यावस्था में है। इसमें CO के 0.3 मोल, H2 के 0.1 मोल H2O के 0.02 मोल एवं CH4 की अज्ञात मात्रा हैं। दिए गए ताप पर अभिक्रिया के लिए Kc का मान 3.90 है। मिश्रण में CH4 की मात्रा ज्ञात कीजिए।
उत्तर:
इस अभिक्रिया के लिए
\(\mathrm{K}_{\mathrm{c}}=\frac{\left[\mathrm{CH}_4\right]\left[\mathrm{H}_2 \mathrm{O}\right]}{[\mathrm{CO}]\left[\mathrm{H}_2\right]^3}\)
V = 1 लीटर अत: मोल ही मोल लीटर 1 होंगे
Kc = 3.90 [CH4] = ?
[H2O] = 0.02
[CO] = 0.30, [H2] = 0.1
मान रखने पर
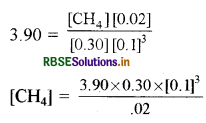
[CH4] = 5.85 × 102 M
प्रश्न 7.35.
संयुग्मी अम्ल-क्षार युग्म का क्या अर्थ है? निम्नलिखित स्पीशीज के लिए संयुग्मी अम्ल/क्षार बताइए- HNO2, CN°, HCIO4, F-, OH-, CO32- एवं S2-
उत्तर:
अम्ल तथा क्षार के एक युग्म में जब एक प्रोटॉन का अन्तर होता है तो इसे संयुग्मी अम्ल क्षार युग्म कहते हैं। अम्ल में से एक प्रोटोन (H+) कम करने पर संयुग्मी क्षार तथा क्षार में एक प्रोटोन जोड़ने पर संयुग्मी अम्ल प्राप्त होता है।
|
HNO2 |
संयुग्मी क्षार NO2- |
OH- |
संयुग्मी अम्ल H2O |
|
CN- |
संयुग्मी अम्ल HCN |
CO32- |
संयुग्मी अम्ल HCO-3 |
|
HClO4 |
संयुग्मी क्षार ClO4- |
S2- |
संयुग्मी अम्ल HS- |
|
F- |
संयुग्मी अम्ल HF |
|
|
प्रश्न 7.36.
निम्नलिखित में से कौनसे लूइस अम्ल हैं?
H2O, BF3, H+ एवं NH4+
उत्तर:
BF3, H+, NH+4 (यहाँ NH+4 अति दुर्बल लूइस अम्ल)
प्रश्न 7.37.
निम्नलिखित ब्रन्स्टेद अम्लों के लिए संयुग्मी क्षारकों के सूत्र लिखिए:
HF, H2SO4 एवं HCO3
उत्तर:
| ब्रन्स्टेव क्षारकों |
संयुग्मी अम्ल |
| HF | F- |
| H2SO4 |
HSO4- |
| HCO3 |
CO32- |
प्रश्न 7.38.
ब्रन्स्टेव क्षारकों NH2-, NH3 तथा HCOO- के संयुग्मी अम्ल लिखिए।
उत्तर:
| ब्रन्स्टेव क्षारकों |
संयुग्मी अम्ल |
| NH2- | NH3 |
| NH3 |
HSO4- |
| HCOO- |
CO32- |
प्रश्न 7.39.
स्पीशीज H2O, HCO-3 HSO4- तथा NH3 ब्रन्स्टेद अम्ल तथा क्षारक दोनों की भाँति व्यवहार करते हैं। प्रत्येक के संयुग्मी अम्ल तथा क्षारक बताइए।
उत्तर:
|
स्पीशीज |
संयुग्मी अम्ल |
संयुग्मी क्षारक |
|
H2O |
H3O+ |
OH- |
|
HCO3- |
H2CO3 |
CO32- |
|
HSO4- |
H2SO4 |
SO42- |
|
NH3 |
NH4+ |
NH2- |
प्रश्न 7.40.
निम्नलिखित स्पीशीज को लूइस अम्ल तथा क्षारक में वर्गीकृत कीजिए तथा बताइए कि ये किस प्रकार लूइस अम्ल-क्षारक के समान कार्य करते हैं: (क) OH (ख) F (ग) H+ (घ) BCl3
उत्तर:
(क) 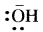 लूइस क्षार है क्योंकि यह इलेक्ट्रॉन युग्म का दान कर सकता है।
लूइस क्षार है क्योंकि यह इलेक्ट्रॉन युग्म का दान कर सकता है।
OH- + H+ → H2O
(ख) 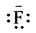 लूइस क्षार है क्योंकि यह इलेक्ट्रॉन युग्म का दान करता है।
लूइस क्षार है क्योंकि यह इलेक्ट्रॉन युग्म का दान करता है।
F- + BF3 → BF-4
(ग) लूइस अम्ल है क्योंकि यह लुइस क्षारक से इलेक्ट्रॉन युग्म ग्रहण कर सकता है।
H+ + OH- → H2O
(घ) BCl3 लूइस अम्ल है क्योंकि यह इलेक्ट्रॉन युग्म ग्रहण कर सकता है।
BCl3 + NH3 → [NH3 → BCl3 ]
प्रश्न 7.41.
एक मृदु पेय के नमूने में हाइड्रोजन आयन की सांद्रता 3.8 x 10-3 M है। उसकी pH परिकलित कीजिए।
उत्तर:
pH = -log [H+]
[H+] = 3.8 × 10-3
अतः
pH = - log (3.8 × 10-3)
pH = -log 3.8 - log 10-3
pH = 0.5798 + 3
pH = 2.4202
(log 3.8 = 0.5798)
pH = 2.42
प्रश्न 7.42.
सिरके के एक नमूने की pH 3.76 है, इसमें हाइड्रोजन आयन की सांद्रता ज्ञात कीजिए।
उत्तर:
log [H+] = - pH
= -3.76
= 4.24
[H+] = Antilog 4.24 (Antilog 0.24 = 1738)
[H+] = 1.738 × 10-4 M

प्रश्न 7.43.
HF, HCOOH तथा HCN का 298K पर आयनन स्थिरांक क्रमश: 6.8 x 10-4, 1.8 x 10-4 तथा 4.8 x 10-9 है। इनके संगत संयुग्मी क्षारकों के आयनन स्थिरांक ज्ञात कीजिए।
उत्तर:
किसी संयुग्मी अम्ल क्षार युग्म के लिए Ka x Kb = Kw (1 × 10-14)
\(\mathrm{K}_{\mathrm{b}}=\frac{\mathrm{K}_{\mathrm{w}}}{\mathrm{K}_{\mathrm{a}}}\)
(i) HF के संयुग्मी क्षारक F के लिए Kb = Kw/Ka
\(=\frac{1 \times 10^{-14}}{6.8 \times 10^{-4}}\)
= 1.47 × 10 = 1.5 x 10-11
(ii) HCOOH के संयुग्मी क्षारक HCOO" के लिए
\(\begin{aligned} & \mathrm{K}_{\mathrm{b}}=\frac{\mathrm{K}_{\mathrm{w}}}{\mathrm{K}_{\mathrm{a}}} \\ & =\frac{1 \times 10^{-14}}{1.8 \times 10^{-4}} \end{aligned}\)
= 5.55 × 10-11 = 5.6 × 10-11
(iii) HCN के संयुग्मी क्षारक CN के लिए
\(\begin{aligned} & \mathrm{K}_{\mathrm{b}}=\frac{\mathrm{K}_{\mathrm{w}}}{\mathrm{K}_{\mathrm{a}}} \\ & =\frac{1 \times 10^{-14}}{4.8 \times 10^{-9}} \end{aligned}\)
= 2.08 x 106
प्रश्न 7.44
फीनॉल का आयनन स्थिरांक 1.0 x 10-10 है। 0.05M फीनॉल के विलयन में फीनॉलेट आयन की सांद्रता तथा 0.01M सोडियम फीनेट विलयन में उसके आयनन की मात्रा ज्ञात कीजिए।
उत्तर:
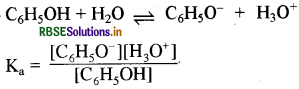
चूँकि [C6H5O-] = [H3O+] अत: [C6H5O-]
\(=\sqrt{\mathrm{K}_{\mathrm{a}} \times\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{OH}\right]}\)
(Ka = 1 × 10-10 [C6H5OH] = 0.05M)
\(=\sqrt{1 \times 10^{-10} \times 0.05}\)
= 2.23 x 10-6
अतः फीनॉलेट आयन की सान्द्रता =
2.23 x 10-6 M
आयनन की मात्रा \(\alpha=\sqrt{\frac{\mathrm{K}_{\mathrm{a}}}{\mathrm{c}}}\)
\(\alpha=\sqrt{\frac{1 \times 10^{-10}}{0.05}}\)
= 4.47 x 10-5
a = 4.47 x 10-5
माना 0.01 M सोडियम फीनेट की उपस्थिति में फीनॉल की आयनन की मात्रा = α
|
प्रारम्भ में |
0.05 |
0.05 |
0 |
|
साम्य पर सान्द्रता |
0.05 - 0.05α |
0.05α |
0.05α |
[C6H5OH] = 0.05 - 0.05α 0.05M ( क्योंकि α का मान नगण्य है।)
[C6H5O] = 0.01 (सोडियम फीनेट से) + 0.05α 0.01 M
[H3O+] = 0.05 αM
अम्ल वियोजन स्थिरांक (Ka) = \(\frac{\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{O}^{-}\right]\left[\mathrm{H}_3 \mathrm{O}^{+}\right]}{\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{OH}\right]}\)
\(\mathrm{K}_{\mathrm{a}}=\frac{(0.01) \times(0.05 \alpha)}{0.05}\)
1 × 10-10 = 01 α
आयनन की मात्रा α = 1 x 10-8
प्रश्न 7.45.
H2S का प्रथम आयनन स्थिरांक 9.1 x 10-8 है। इसके 0.1M विलयन में HS- आयनों की सांद्रता की गणना कीजिए तथा बताइए कि यदि इसमें 0.1 MHCl भी उपस्थित हो, तो यह सांद्रता किस प्रकार प्रभावित होगी, यदि H2S का द्वितीय वियोजन स्थिरांक = 1.2 x 10-13 हो, तो S2 ( सल्फाइड) आयनों की दोनों स्थितियों में सांद्रता की गणना कीजिए।
उत्तर:
(i) [HS-] की गणना 
|
प्रारम्भ में |
0.1 |
0 |
0 |
|
साम्य पर सान्द्रता |
0.1 - x |
x |
x |
(माना साम्य पर H2S के x मोल वियोजित होते हैं)
[H2S] = 0.1 x 0.1M
अत: \(\mathrm{K}_{\mathrm{a}_1}=\frac{\left[\mathrm{H}^{+}\right]\left[\mathrm{HS}^{-}\right]}{\left[\mathrm{H}_2 \mathrm{~S}\right]}\)
(Ka = 9.1 × 10-8), 9.1 × 10-8 = 
2 = 9.1 × 10-9
[H+] = [HS-] = x = 9.539 × 10-5 M
(ii) 0.1 M HCl की उपस्थिति में HS की सान्द्रता
(माना 0.1M HCl की उपस्थिति में H2S के y मोल वियोजित होते हैं)
[H2S] = 0.1 - y = 0.1 M
[H+] = y + 0.1 (HCI से) 0.1M
\(\mathrm{K}_{\mathrm{a}_1}=\frac{\left[\mathrm{H}^{+}\right]\left[\mathrm{HS}^{-}\right]}{\left[\mathrm{H}_2 \mathrm{~S}\right]}=\frac{(0.1) \mathrm{y}}{0.1}\)
[HS-] = y = 9.1 x 10-8 M
(iii) S-2 की सान्द्रता की गणना
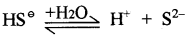
K2 = 1.2 x 10-15
[H+] = [HS-] = 9.54 x 10-5 M ( प्रथम वियोजन से )
क्योंकि द्वितीय वियोजन बहुत कम होता है अतः उससे प्राप्त [H+] को नगण्य माना जा सकता है।

[S2-] = 1.2 × 10-13 M
(iv) 0.1M HCl की उपस्थिति में S2- की सान्द्रता की गणना
[HS-] = 9.1 × 10-8 M (ii से)
[H+] = 0.1 (HCl से, HS- से प्राप्त [H+] = नगण्य)
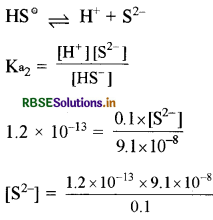
[S2-] = 1.09 × 10-19 M

प्रश्न 7.46.
एसिटिक अम्ल का आयनन स्थिरांक 1.74 x 10-5 है। इसके 0.05M विलयन में वियोजन की मात्रा, ऐसीटेट आयन सांद्रता तथा pH का परिकलन कीजिए।
उत्तर:
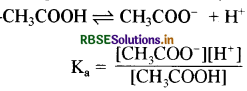
CH3COOH दुर्बल अम्ल है अतः इसका आयनन बहुत कम होगा इसलिए इसकी प्रारम्भिक सान्द्रता को ही साम्य सान्द्रता मानेंगे तथा
[CH3COO-] = [H+]
अतः \(\mathrm{K}_{\mathrm{a}}=\frac{\left[\mathrm{H}^{+}\right]^2}{\left[\mathrm{CH}_3 \mathrm{COOH}\right]},\left[\mathrm{H}^{+}\right]=\sqrt{\mathrm{K}_{\mathrm{a}}\left[\mathrm{CH}_3 \mathrm{COOH}\right]}\)
\(\left[\mathrm{H}^{+}\right]=\sqrt{1.71 \times 10^{-5} \times(0.05)}\)
[H+] = [CH3COO-] = 9.327 × 10-4 = 9.33 × 10-4 M
= 0.00093 M
विलयन की pH = -log [H+]
pH = - log (10-4 x 9.33)
= 4 - 0.9699
(log 9.33 = 0.9699) pH = 3.03
प्रश्न 7.47
0.01M कार्बनिक अम्ल (HA) के विलयन की pH 4.15 है। इसके ऋणायन की सांव्रता, अम्ल का आयनन स्थिरांक तथा pKa मान परिकलित कीजिए।
उत्तर:
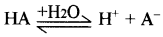
या
pH = - log [H+]
log [H'] = - pH = - 4.15 = 5.85
[H] = antilog 5.85 = 7.079 x 10-5 M (Antilog 0.85 7079)
[A-] = [H+]= 7.079 x 10-5 M = 7.08 × 10-5
अतः
आयनन स्थिरांक
\(\mathrm{K}_{\mathrm{a}}=\frac{\left[\mathrm{H}^{+}\right]\left[\mathrm{A}^{-}\right]}{[\mathrm{HA}]}\)
[HA] = 0.01
\(\mathrm{K}_{\mathrm{a}}=\frac{\left(7.08 \times 10^{-5}\right)^2}{0.01}\)
Ka = 5.08 × 10-7
PKa = -log Ka
PKa = -log (5.08 x 10-7)
PKa = 7 - 0.7059 (log 5.08 = 0.7059)
PKa = -6.29
प्रश्न 7.48.
पूर्ण वियोजन मानते हुए निम्नलिखित विलयनों के pH ज्ञात कीजिए:
(क) 0.003M HCI
(ख) 0.005 M NaOH
(ग) 0.002 M HBr
(घ) 0.002 M KOH
उत्तर:
(क) [H+] = [HCl] = 3 × 10-3
pH = -log [H+],
pH = -log (10-3 x 3)
pH = 3 - log 3
(log 3 = 0.4778)
pH = 3-0.4778
pH = 2.5222 ≈ 2.52
(ख) [OH] = [NaOH] = 0.005 = 5 x 10-3
Kw = [H] [OH-]
[H+] = Kw/(OH-)
[H+] = 1-10-14/5 x 10-3
[H+] = 2 × 10-12
pH = -log (10-12 x 2)
pH = 12 - log 2
pH = 11.70
(log 2 = 0.3010)
(ग) [H+] = [HBr] = 0.002 = 2 x 10-3
pH = -log [H+],
pH = -log (2 × 10-3)
pH = 3 - log 2
(log 2 = 0.3010)
pH = 2.6990 = 2.70
(घ) [KOH] = [OH-] = 0.002 = 2 × 10-3
[H+] = 1 x 10-14/2 x 10-3
[H+] = 5 x 10-12
pH = -log (10-12 x 5)
pH = 11.36
(log 5 = 0.6990)

प्रश्न 7.49.
निम्नलिखित विलयनों के pH ज्ञात कीजिए:
(क) 2 ग्राम TIOH को जल में घोलकर 2 लिटर विलयन बनाया जाए।
(ख) 0.3 ग्राम Ca(OH)2 को जल में घोलकर 500 ml विलयन बनाया जाए।
(ग) 0.3 ग्राम NaOH को जल में घोलकर 200 mL विलयन बनाया जाए।
(घ) 13.6 M HCl के 1mL को जल से तनुकरण करके कुल आयतन 1 लिटर किया जाए।
उत्तर:
(क) TIOH की मोलरता

(TIOH का मोलर द्रव्यमान = 221)
\(\mathrm{M}=\frac{2(\mathrm{~g})}{221 \mathrm{~g} \mathrm{~mol}^{-1} \times 2(\mathrm{~L})}\)
= 4.52 × 10-3 M
[OH-] = [TIOH] = 4.52 x 10-3 M
(100% आयनन मानेंगे)
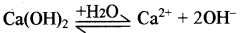
= 4.52 x 10-3
pH = - log [H+]
PH = - log (2.21 x 10-12)
pH = 12 - log 2.21 (log 2.21 = 0.3424 )
pH = 12 - 0.3424 = 11.65
(ख) Ca(OH)2 की मोलरता
\((\mathrm{M})=\frac{0.3 \mathrm{~g}}{74 \mathrm{~g} \mathrm{~mol}^{-1} \times 0.5 \mathrm{~L}}\)
(Ca(OH)2 का मोलर द्रव्यमान = 74)
( V = 500ml = 0.5 L)
M = 8.108 × 10 M
(100% आयनन मानेंगे) [OH-] = 2 × M
[OH ] = 1.6216 × 10-2
\(\left[\mathrm{H}^{+}\right]=\frac{10^{-14}}{1.6216 \times 10^{-2}}\)
= 6.166 × 10-13
pH = - log [H+]
pH = log (6.166 x 10-13)
pH = 13 - log 6.166 (log 6.166 = 0.7830)
pH = 13 - 0.7830
pH = 12.21
(ग) NaOH की सान्द्रता
\([\mathrm{M}]=\frac{0.3 \mathrm{~g}}{40 \mathrm{~g} \mathrm{~mol}^{-1} \times 0.2 \mathrm{~L}}\) = 3.75 x 10-2
(V = 200 ml = 0.2 L)
(NaOH का मोलर द्रव्यमान = 40)
[NaOH] = [OH-] = 3.75 x 10-2
(प्रबल क्षार)
[H] = 10-14/3.75 x 10-2
= [H] 2.66 x 10-13
PH = log 10-13 - log 2.66
pH = 13 - 0.4249
pH = 12.57 (log 2.66 = 0.4249)
(घ) HCl के लिए MN ( नार्मलता )
N1V1 = N2V2
N1 = 13.6 N2? V1 = 1 ml
V2 = 100 mL (1 efter)
आयतन बढ़ाने से सान्द्रता कम हो जाएगी
13.6 × 1 = N2 × 1000
N2 = 1.36 x 10-2
(HCl)= [H+] = N2 = 1.36 × 10-2
pH = -log (1.36 × 10-2)
pH = 2 - log 1.36 (log 1.36 = 0.1335)
pH = 2 - 0.1335
pH = 1.866
pH = 1.87
प्रश्न 7.50.
ब्रोमोएसीटिक अम्ल की आयनन की मात्रा 0.132 है 1 0.1M अम्ल की pH तथा pK का मान ज्ञात कीजिए।
उत्तर:
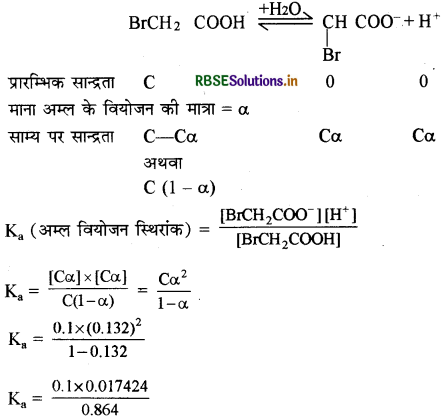
Ka = 2.02 × 10-3
PKa = -log Ka
PKa = log (2.02× 10-3)
PKa = 3 - log 2.02
PKa = 3 0.3054
PKa = 2.69
PKa = 2.70
[log 2.02 = 0.3054]
[H+] = Ca (उपर्युक्त व्युत्पन्न के अनुसार)
[H+] = 0.1 0.132 = 1.32 x 10-2 M
pH = -log [H+]
= -log (1.32 × 10-2)
pH = 2 - log 1.32
pH = 2 - 0.1206 = 1.88 (log 1.32 = 0.1206) pH = 1.879 = 1.88
प्रश्न 7.51
0.005M कोडीन (C18H21NO2) विलयन की pH 9.95 है। इसका आयनन स्थिरांक तथा pKb ज्ञात कीजिए।
उत्तर:
कोडीन की pH = 9.95
अतः pOH = 14 - 9.95 = 4.05
अतः log [OH] = - pOH = 4.05 = 3.95
[OH-] = Antilog 3.95
= [OH-] = 8.91 x 10-5 (Antilog 0.95 = 8910)
कोडीन एक क्षार (B) है अतः इसका आयनन निम्न प्रकार होगा:
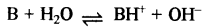
क्षार वियोजन स्थिरांक (Kb)
\(=\frac{\left[\mathrm{OH}^{-}\right]^2}{[\mathrm{~B}]}\)
(कोडीन [OH-] = [BH+])
\(\mathrm{K}_{\mathrm{b}}=\frac{\left(8.91 \times 10^{-5}\right)^2}{0.005}\)
= 1.58 × 10-6
= 1.6 x 10-6
Kb = 1.6 x 106
PK = -log Kь = -log (1.6 × 10-6)
PKь = 6-log 1.6
(log 1.6 = 0.2041)
PKb = 6 - 0.2041
PKb = 5.8
प्रश्न 7.52
0.001M एनीलीन विलयन का pH क्या है? एनीलीन का आयनन स्थिरांक सारणी 7.7 ( पाठ्यपुस्तक) से ले सकते हैं। विलयन में एनीलीन के आयनन की मात्रा की गणना कीजिए। इसके संयुग्मी अम्ल का आयनन स्थिरांक भी ज्ञात कीजिए।
उत्तर:
एनीलीन (क्षार) का आयनन स्थिरांक (सारणी 7.7 से)
Kь = 4.27 x 10-10 तथा [C6H5NH2] = 0.001
= 10-3 M
एनीलीन दुर्बल क्षार है जिसका आयनन निम्न प्रकार होगा:
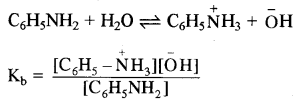
चूँकि [C6H5NH3 ][ [OH)
अत: \(\mathrm{K}_{\mathrm{b}}=\frac{[\overline{\mathrm{O} H}]^2}{\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{NH}_2\right]}\)
[OH-] = \(\sqrt{\mathrm{K}_{\mathrm{b}} \times\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{NH}_2\right]}\)
[OH-] = \(\sqrt{\left.4.27 \times 10^{-10} \times 10^{-3}\right]}\)
[OH-] = 6.534 × 10-7 M
\(\left[\mathrm{H}^{+}\right]=\frac{\mathrm{K}_{\mathrm{w}}}{\left[\mathrm{OH}^{-}\right]}=\frac{10^{-14}}{6.534 \times 10^{-7}}\)
[H+] = 1.53 × 108
pH = log (1.53 × 10-8)
pH = 8 - log 1.53
(log 1.53 = 0.1847)
pH = (8 - 0.1847)
pH = 7.8150 = 7.82
दुर्बल क्षार (एनीलीन) के लिए आयनन की मात्रा
\(\alpha=\sqrt{\frac{\mathrm{K}_{\mathrm{b}}}{\mathrm{C}}}=\sqrt{\frac{4.27 \times 10^{-10}}{10^{-3}}}\)
= 6.53 × 10-4
α = 6.53 x 10-4
संयुग्मी अम्ल क्षार युग्म के लिए, Ka x Kb = Kw
\(\mathrm{K}_{\mathrm{a}}=\frac{\mathrm{K}_{\mathrm{w}}}{\mathrm{K}_{\mathrm{b}}}=\frac{1 \times 10^{-14}}{4.27 \times 10^{-10}}\)
आयनन स्थिरांक
Ka = 2.34 x 105

प्रश्न 7.53.
यदि 0.05M ऐसीटिक अम्ल के pK का मान 4.74 है, तो आयनन की मात्रा ज्ञात कीजिए। यदि इसे (अ) 0.01M HCl (ब) 0.1M HCl विलयन में डाला जाए, तो वियोजन की मात्रा किस प्रकार प्रभावित होती है?
उत्तर:
एसीटिक अम्ल का pKa = 4.74
- log Ka = pKa
log Ka = - PKa = -4.74 = 3.26
Ka = Antilog 3.26
Ka = 1.82 x 10-5
(Antilog 0.26 = 1820)
CH3COOH (दुर्बल अम्ल) के लिए
आयनन की मात्रा \((\alpha)=\sqrt{\frac{\mathrm{K}_{\mathrm{e}}}{\mathrm{c}}}=\sqrt{\frac{1.82 \times 10^{-5}}{0.05}}\)
(c = 0.05)
α = 1.9 × 10-2
(अ) प्रबल अम्ल (HCl) की उपस्थिति में समआयन प्रभाव के कारण CH3COOH का आयनन कम हो जाता है।
0.01 M HCl की उपस्थिति में
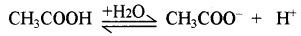
|
प्रारम्भिक सान्द्रता |
0.05 |
0 |
0 |
|
साम्य पर सान्द्रता |
0.05 – 0.05 α |
0.05α |
0.05α |
(α = आयनन की मात्रा )
[CH3COOH] = 0.05 - 0.05 α
= 0.05 M
(0.05 α << 0.05)
[H] = 0.01 + 0.05 a (0.05 α << 0.01)
(HCl)
[H+] = 0.01 M
[CH3COO-] = 0.05 a
\(\begin{aligned} & \mathrm{K}_{\mathrm{a}}=\frac{\left[\mathrm{CH}_3 \mathrm{COO}^{-}\right]\left[\mathrm{H}^{+}\right]}{\left[\mathrm{CH}_3 \mathrm{COOH}\right]} \\ & 1.82 \times 10^{-5}=\frac{(0.05 \alpha) \times 0.01}{0.05} \end{aligned}\)
α = 1.82 x 103 = 0.0018
(ब) 0.1M HCI की उपस्थिति में
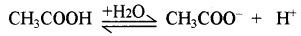
|
प्रारम्भिक सान्द्रता |
0.05 |
0 |
0 |
|
साम्य पर सान्द्रता |
0.05 – 0.05 α |
0.05α |
0.05α |
[CH3COOH] = 0.05 - 0.05 a ≈ 0.05
[CH3COOH] = 0.05 α, [H+] = 0.05 a + 0.1 (HCl) ≈ 0.1
\(\begin{aligned} & \mathrm{K}_{\mathrm{a}}=\frac{\left[\mathrm{CH}_3 \mathrm{COO}^{-}\right]\left[\mathrm{H}^{+}\right]}{\left[\mathrm{CH}_3 \mathrm{COOH}\right]} \\ & =\frac{(0.05 \alpha) \times(0.1)}{0.05} \end{aligned}\)
α = 1.82 × 10-4
= 0.00018
प्रश्न 7.54.
डाइमेथिल एमीन का आयनन स्थिरांक 5.4 × 10-4 है। इसके 0.02M विलयन की आयनन की मात्रा की गणना कीजिए । यदि यह विलयन NaOH में भी 0.1M हो तो डाइमेथिल एमीन का प्रतिशत आयनन क्या होगा?
उत्तर:
डाइमेथिल एमीन दुर्बल क्षार है, इसके लिए
आयनन की मात्रा α = \(\sqrt{\frac{\mathrm{K}_{\mathrm{b}}}{\mathrm{c}}}\)
Kb = 5.4 × 10 + c = 0.02 M
\(\alpha=\sqrt{\frac{5.4 \times 10^{-4}}{0.02}}\)
= 0.164
माना 0.1M NaOH की उपस्थिति में आयनन की मात्रा a' है तो
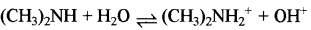
|
प्रारम्भिक सान्द्रता |
0 |
0 |
0 |
|
साम्य पर सान्द्रता |
0.02 – 0.02α |
0.02α |
0.02α + 0.1 |
(NaOH से)
[(CH3)2NH| = 0,02 - 0,02 α
[OH ] = 0.02 α + 0.1 = 0.1
[(CH3)2NH2+] = 0.02 α1
\(\mathrm{K}_{\mathrm{b}}=\frac{\left[\left(\mathrm{CH}_3\right)_2 \mathrm{NH}_2^{+}\right]\left[\mathrm{OH}^{-}\right]}{\left(\mathrm{CH}_3\right)_2 \mathrm{NH}}=\frac{\left(0.02 \alpha^1\right)(0.1)}{0.02}\)
आयनन की मात्रा α = 5.4 × 10 = 0,0054
प्रतिशत आयनन = 0.0054 x 100 = 0.54%
प्रश्न 7.55.
निम्नलिखित जैविक द्रवों, जिनमें pH दी गई है की हाइड्रोजन आयन सांद्रता परिकलित कीजिए:
(क) मानव पेशीय द्रव, 6.83
(ख) मानव उदर द्रव, 1.2
(ग) मानव रुधिर 7.38
(घ) मानव लार, 6.4
उत्तर:
(क) (मानव पेशीय द्रव)
pH = -log [H+]
log [H+] = - pH = - 6.83 = 7.17
[H+] = antilog 7.17 = 1.48 × 10-7 M
(Antilog 0.17 = 148)
(ख) (मानव उदर द्रव)
log [H+] = - 1.2 = 2.8
[H+] = antilog ( 28 ) = 6.31 × 10-2 M
(Antilog 0.8 = 631)
= 0.063 M
(ग) (मानव रुधिर)
log [H+] = - 7.38 = 8.62
[H+] = antilog 8.62
= 4.17 × 10-8 M
(Antilog 0.62 = 417)
(घ) (मानव लार)
log [H+] = -6.4 = 7.6
[H+] = antilog (7.6) = 3.98 × 10-7 M
(Antilog 0.6 = 398)
प्रश्न 7.56.
दूध, कॉफी, टमाटर रस, नींबू रस तथा अंडे की सफेदी के pH का मान क्रमश: 6.8, 5.0, 4.2, 2.2 तथा 7.8 है। आयन की सांद्रता ज्ञात कीजिए। दूध की pH = 6.8
प्रत्येक के संगत H+
उत्तर:
(क)
log [H+] = - pH
= - 6.8 = 7.2
[H+] = Antilog 7.2 = 1.585 x 10-7 M
(antilog 0.2 = 1585)
(ख) कॉफी की pH = 5.0
log [H+] = pH = - 50 = 3.00
[H+] = antilog 3.00
= 1 × 10-5 M
(antilog 0.0 = 1 )
(ग) टमाटर रस की pH = 4.2
log [H+] = pH = - 4.2 = 3.8
[H] = Antilog 3.8 = 6.31 x 10-3 M
(antilog 0.8 = 631)
(घ) नींबू रस की pH = 2.2
log [H+] = pH = - 2.2 = 3.8
[H+] = Antilog 3.8 = 6.31 x 10-3 M
(antilog 0.8 = 631)
(ङ) अण्डे की सफेदी की pH = 7.8
log [H+] = - pH = 78 = 8.2
[H+] = Antilog 8.2 = 1.585 × 10-8 M
(antilog 0.2 = 1585)
प्रश्न 7.57.
298K पर 0.561g, KOH जल में घोलने पर प्राप्त 200 ml विलयन की pH पोटैशियम हाइड्रोजन तथा हाइड्रॉक्सिल आयनों की सांवताएँ ज्ञात कीजिए।
उत्तर:
सान्द्रता M (मोल L-1 )

(KOH का मोलर द्रव्यमान 56g mol-1 M = \(\frac{0.561}{56}\) x 100
= 0.05 M
KOH प्रबल क्षार है अतः जलीय विलयन में इसका पूर्ण आयनन
अतः [K+] = [KOH] [OH-] = 0.05 M
\(\left[\mathrm{H}^{+}\right]=\frac{\mathrm{K}_{\mathrm{w}}}{\left[\mathrm{OH}^{-}\right]}=\frac{1 \times 10^{-14}}{0.05}\)
= 2 × 10-13 M
pH = - log [H+] = - log (2 × 10-13)
pH = 13 - log 2
pH = 12.7
(log 2 = 0.3010)

प्रश्न 7.58.
298K पर Sr (OH)2 विलयन की विलेयता 19.23 g/L है। स्ट्रांशियम तथा हाइड्रॉक्सिल आयन की सांद्रता तथा विलयन की pH ज्ञात कीजिए।
उत्तर:
Sr(OH)2 का मोलर द्रव्यमान = 87.6 + (162) + (1 × 2)
= 121.6 g mol-1
Sr(OH)2 की मोलरता
\(=\frac{19.23 \mathrm{~g}}{121.6 \mathrm{~g} \mathrm{~mol}^{-1} \times 1(\mathrm{~L})}\)
= 0.1581 mol L1
100% आयनन मानते हुए Sr2+ की सान्द्रता =
=[Sr2+] = 0.1581M
अतः [OH-] = 2 × 0.1581 = 0.3162 M
क्योंकि 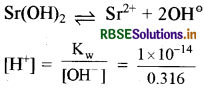
= 3.165 × 10-14 mol L-1
pH = - log [H' ] = - log ( 3.165 x 10-14)
pH = 14 - log 3.165
pH = 13.50 (log 3.165 = 0.5 )
प्रश्न 7.59
प्रोपेनोइक अम्ल का आयनन स्थिरांक 1.32 x 10-5 है 0.05M अम्ल विलयन के आयनन की मात्रा तथा pH ज्ञात कीजिए। यदि विलयन में 0.01 M HCl मिलाया जाए तो उसके आयनन की मात्रा ज्ञात कीजिए।
उत्तर:
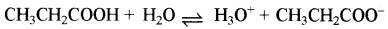
|
प्रारम्भिक सान्द्रता |
0.05 M |
0 |
0 |
|
साम्य पर सान्द्रता |
0.05 – 0.05α |
0.05α |
0.05α |
( माना अम्ल के आयनन की मात्रा = α )
\(\begin{aligned} \mathrm{K}_{\mathrm{a}} & =\frac{\left[\mathrm{H}_3 \mathrm{O}^{+}\right]\left[\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{COO}^{-}\right]}{\left[\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{COOH}\right]} \\ & =\frac{(0.05 \alpha)(0.05 \alpha)}{0.05} \end{aligned}\)
1.32 x 10-5 = 0.05 α2
\(\alpha=\sqrt{\frac{1.32 \times 10^{-5}}{0.05}}\)
= 1.63 x 10-2
[H3O+] = Cα
[H3O+] [H+] = 0.05α = 0.05 x 1.63 × 10-2
[H+] = 8.15 104 M
pH = -log [H+]
= -log 8.15 x 10-4
pH = 4 - log 8.15
pH = 4 - 0.91 = 3.09
(log 8.15 = 0.91)
माना 0.01 M HCl की उपस्थिति में प्रोपेनोइक अम्ल की आयनन की मात्रा = α
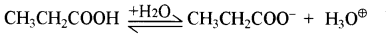
|
प्रारम्भिक सान्द्रता |
0.05 M |
0 |
0 |
|
साम्य पर सान्द्रता |
0.05 – 0.05α1 |
0.05α |
0.05α1 |
\(\begin{aligned} & =\frac{\left[\mathrm{H}_3 \mathrm{O}^{+}\right]\left[\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{COO}^{-}\right]}{\left[\mathrm{CH}_3 \mathrm{CH}_2 \mathrm{COOH}\right]} \\ & =\frac{0.01 \times 0.05 \alpha^1}{0.05} \end{aligned}\)
= 1.32 × 10-3
प्रश्न 7.60.
यदि साइनिक अम्ल (HCNO) के 0.1M विलयन की pH 2.34 हो, तो अम्ल के आयनन स्थिरांक तथा आयनन की मात्रा ज्ञात कीजिए।
उत्तर:
pH = - log [H+]
log [H+] = - pH = -2.34 = 3.66
[H+] = antilog (3.66) = 4.57 10-3 M (antilog 0.66 = 457)
HCNO दुर्बल अम्ल है अतः इसके लिए
[H+] = cα
आयनन की मात्रा α = \(\frac{\left[\mathrm{H}^{+}\right]}{\mathrm{c}}=\frac{4.57 \times 10^{-3}}{0.1}\)
= 4.57 x 10-2 =
= 0.0457
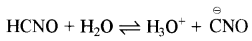
आयनन स्थिरांक \(\left(\mathrm{K}_{\mathrm{a}}\right)=\frac{\left[\mathrm{H}_3 \mathrm{O}^{+}\right]^2}{[\mathrm{HCNO}]}\)
\(\mathrm{K}_{\mathrm{a}}=\frac{\left[\mathrm{H}_3 \mathrm{O}^{+}\right]^2}{\mathrm{C}} \mathrm{K}_{\mathrm{a}}=\frac{\left(4.57 \times 10^{-3}\right)^2}{0.1} \)
= 2.088 × 10-4 = 2.09 × 10-4
प्रश्न 7.61.
यदि नाइट्स अम्ल का आयनन स्थिरांक 4.5 x 10 है, तो 0.04M सोडियम नाइट्राइट विलयन की pH तथा जलयोजन की मात्रा ज्ञात कीजिए।
उत्तर:
सोडियम नाइट्राइट (NaNO2), प्रबल क्षार (NaOH) तथा दुर्बल अम्ल (HNO2) से बना लवण है तथा इसके लिए जल अपघटन की मात्रा = h
\(\mathbf{h}=\sqrt{\frac{\mathrm{K}_{\mathrm{w}}}{\mathrm{K}_{\mathrm{a}} \times \mathrm{c}}}=\sqrt{\frac{1 \times 10^{-14}}{4.5 \times 10^{-4} \times 0.04}}\)
(c = 0.04M, Kg = 4.5 × 10-4)
pH का सूत्र (WA + SB)
pH = 1/2[pKw + pKa + log c]
pH = 1⁄2 [14 - log (4.5 × 10-4) + log 0.04]
pH = 1/2[14 + 3.3468 - 1.398]
(log 4.5 = 0.6532 तथा log 0.04 = - 1.398)
pH = 7.97
प्रश्न 7.62.
यदि पिडिनियम हाइड्रोजन क्लोराइड के 0.02M विलयन का pH 3. 44 है, तो पिरीडीन का आयनन स्थिरांक ज्ञात कीजिए।
उत्तर:
पिरीडिनियमहाइड्रोजनक्लोराइड दुर्बल क्षार 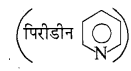 तथा प्रबल अम्ल (HCI) का लवण है अतः इसके जलीय विलयन का pH-
तथा प्रबल अम्ल (HCI) का लवण है अतः इसके जलीय विलयन का pH-
pH = 1⁄2 (pkw - pKb - log c)
PH = 3.44 c = 0.02
3.44 = 1/2(14+ log Kb - log 0.02)
6.88 = 14 + log Ko + 1.7
log Kb = 6.88 - 14 - 1.7
log Kb = - 8.82 = 9.18
Kb = antilog 9.18 = 1.5 x 109
Kb = 1.5 × 10-9
anti log 0.18 = 15
प्रश्न 7.63.
निम्नलिखित लवणों के जलीय विलयनों के उदासीन, अम्लीय तथा क्षारीय होने की प्रागुक्ति (Prediction ) कीजिए:
NaCl, KBr, NaCN, NH4NO3, NaNO2 तथा KF
उत्तर:
यौगिक
उदासीन विलयन
NaCl, KBr (प्रबल अम्ल तथा प्रबल क्षार के लवण)
अम्लीय विलयन
NH4NO3 (प्रबल अम्ल HNO तथा दुर्बल क्षार NH4OH का लवण)
क्षारीय विलयन
NaCN, NaNO2, KF (दुर्बल अम्ल तथा प्रबल क्षार के लवण)
प्रश्न 7.64.
क्लोरोएसीटिक अम्ल का आयनन स्थिरांक 1.35 × 10-3 है। 0.1M अम्ल तथा इसके 0.1M सोडियम लवण की PH ज्ञात कीजिए।
उत्तर:
क्लोरोएसिटिक अम्ल (दुर्बल अम्ल) के लिए
(a)
[H+] = \(\sqrt{\mathrm{K}_{\mathrm{a}} \times \mathrm{c}}\)
Ka = 1.35 × 10-3, c = 0.1M
[H+] = \(\sqrt{1.35 \times 10^{-3} \times 0.1}\)
[H+] = 1.16 × 10-2 M
pH = -log [H+] = - log (1.16 x 10-2)
pH = 2 - log 1.16
(log 1.16 = 0.06)
pH = 2 - 0.06m
(b) क्लोरोएसीटिक अम्ल, CH3COOH (WA) तथा
NaOH (SB) से बना लवण है अतः इसके जलीय विलयन की pH:
pH = 1/2 [pKw + pKa + log c]
Ka = 1.35 x 103, c = 0.1, pKw = 14
pH = 1/2 [14 - log (1.35 x 10-3) + log (0.1)]
= 1/2[14+ + (3 - log 1.35) - 1]
(log 1.35 = 0.1303)
= 1/2[14 + (3 - 0.1303) - 1]
= 1/2 [14 + 2.8697 - 1]
= 1/2[15.8697]
pH = 7.93485 = 7.94
प्रश्न 7.65
310K पर जल का आयनिक गुणनफल 2.7 x 10-14 है। इसी तापक्रम पर उदासीन जल की pH ज्ञात कीजिए।
उत्तर:
जल का आयनिक गुणनफल
Kw = [H2O+] [OH-]
Kw = [H3O+]2
[H3O+] = \(\sqrt{\mathrm{K}_{\mathrm{w}}}=\sqrt{2.7 \times 10^{-14}}\)
= 1.643 x 10-7 mol-1
pH = -log [H] = - log [H2O']
= -log (1.643 x 10-7)
= 7 log (1.643) (log 1.643 = 0.2156)
pH = 7 - 0.2156 = 6.78
pH = 6.78
प्रश्न 7.66.
निम्नलिखित मिश्रणों की pH परिकलित कीजिए:
(क) 0.2M Ca(OH)2 10 mL + 0.1M HCl
(ख) 0.01M H2SO4 10 mL + 0.01M Ca(OH)2 ch 10 mL
(ग) 0.1M H2SO4 10 mL + 0.1M KOH 10 mL
उत्तर:
(क) 0.2 M Ca(OH)2 (10 ml) = MV मिलीमोल
= 0.2 × 10
= 2 मिलीमोल
0.1 M HCI (25 ml) M x V = 0.1 x 25
= 2.5 मिलीमोल
Ca(OH)2 (क्षार) तथा HCI ( अम्ल) मिलकर लवण बनाते हैं।
Ca(OH)2 + 2 HCl → CaCl2 + 2H2O
1 मिलीमोल 2 मिलीमोल
अभिक्रिया की रससमीकरणमिति के अनुसार HCI के 2.5 मिलीमोल, Ca(OH)2 के 1.25 मिलीमोल से क्रिया करेंगे तथा 0.75 मिलीमोल (2 - 1.25 ) Ca(OH)2 बच जाएँगे।
विलयन (मिश्रण) का कुल आयतन 10 + 25
= 35ml
अतः मिश्रण में शेष बचे Ca(OH)2 विलयन की मोलरता:
0.75 मिलीमोल 35 मिली
= 0.0214 M
Ca(OH)2 से प्राप्त [OH] = 2 x 0.0214 = 0.0428
= 4.28 × 102
POH = - log [OH ]
log (4.28 × 10-2)
pOH = 2 - log 4.28
pOH = 2 - 0.6314 (log 4.28 = 0.6314)
POH = 1.37
pH = 14 - pOH = 14 - 1.37 = 12.63
pH = 12.63
(ख) H2SO4 के मिलीमोल= 10 x 0.01 = 0.1
Ca(OH)2 के मिलीमोल = 10 x .01 = 0.1
Ca(OH)2 + H2SO4 → CaSO4 + 2H2O
मिश्रण में Ca(OH)2 तथा H2SO4 के मिली मोल बराबर हैं
अतः विलयन उदासीन होगा अतः
pH = 7
(ग) H2SO4 के मिलीमोल= 10 x 0.1 = 1
KOH के मिलीमोल = 10 × 0.1 = 1
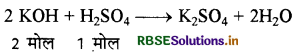
संतुलित समीकरण के अनुसार 1 मिलीमोल KOH,
0.5 मिलीमोल H2SO4 से क्रिया करेगा तथा 0.5 मिलीमोल H2SO4 शेष बचेगा जिसकी मोलरता
= \(\frac{0.5}{20}\) = 2.5 × 10-2
मिश्रण का कुल आयतन = 20ml
H2SO4 से [H+] = 2 × मोलरता = 2 x 2.5 x 10-2
[H+] = 5 × 10-2
pH = -log [H+] = -log (5 × 10-2)
pH = 2 - log 5 (log 5 = 0.6990)
pH = 1.3

प्रश्न 7.67.
सिल्वर क्रोमेट, बेरियम क्रोमेट, फेरिक हाइड्रॉक्साइड, लेड क्लोराइड तथा मर्क्युरस आयोडाइड विलयन की सारणी 7.9 ( पाठ्यपुस्तक) में दिए गए विलेयता गुणनफल स्थिरांक की सहायता से विलेयता ज्ञात कीजिए तथा प्रत्येक आयन की मोलरता भी ज्ञात कीजिए।
(i) Ag2CrO4 Kp = 1.1 × 10-12 (सिल्वर क्रोमेट)
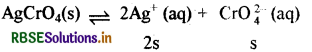
Ksp = [Ag+]2 [CrO42-]
Kp = (2s)2 (s)
Ksp = 4s3, s3 = \(\frac{K_{s p}}{4}\)
\(\mathrm{s}=\sqrt[3]{\frac{\mathrm{K}_{\mathrm{sp}}}{4}}=\left(\frac{1.1 \times 10^{-12}}{4}\right)^{\frac{1}{3}}\)
s = 0.65 x 10-4 M
[Ag+] = 2 x s = 2 × 0.65 × 10-4
= 1.3 x 10-4 M
[CrO42-] = 0.65 x 10-4 M
(ii) बेरियम क्रोमेट (BaCrO4) का Ksp
= 1.2 × 10-10
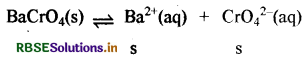
Ksp = [Ba2+] [CrO24-] = s x s = s2
\(\mathrm{s}=\sqrt{\mathrm{K}_{\mathrm{sp}}}=\sqrt{1.2 \times 10^{-10}}\)
= 1.09 × 10-5
= 1.1 × 10-5
अतः [Ba2+] = [CrO42-] = 1.1 x 10-5 M
(iii) फेरिक हाइड्रॉक्साइड [Fe(OH)3] का Ksp
= 1.0 × 10-38
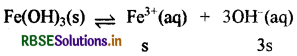
Kp = [Fe3+] [OH-]3
kSP = s x (3S)3
Ksp = 27 s4
\(s^4=\frac{K_{\text {sp }}}{27}=\frac{1 \times 10^{-38}}{27}\)
\(\mathrm{s}=\left(\frac{1 \times 10^{-38}}{27}\right)^{\frac{1}{4}}\)
= 1.39 × 10-10 M = [Fe+3]
[OH-] = 3 x s = 3 × 1.39 × 10-10
(iv) लेड क्लोराइड (PbCl2) Ksp = 1.6 × 10-5
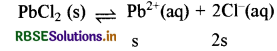
Ksp = [Pb2+] [Cl-]2
s x 2s
Ksp = 4s3, s3 = \(\frac{K_{\text {sp }}}{4}, \quad s=\sqrt[3]{\frac{K_{\text {sp }}}{4}}\)
\(s=\sqrt[3]{\frac{1.6 \times 10^{-5}}{4}}\)
= 1.59 x 10-2 M
[Pb2+] = 1.59 x 10-2 M
[Cl-] = 28 = 2 x 1.59 10-2 = 3.18 x 102M
(v) मर्क्युरस आयोडाइड (Hg2I2) Ksp = 4.5 × 10-29
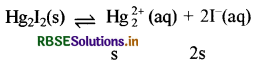
Ksp = [Hg22+][I-]2 = (s) (2s)2 = 4s3
\(\mathrm{s}=\sqrt[3]{\frac{\mathrm{K}_{\mathrm{sp}}}{4}}=\left(\frac{4.5 \times 10^{-29}}{4}\right)^{\frac{1}{3}}\)
= 2.24 × 10-10 M
[I-] = 2S = 2 × 2.24 × 10-10 = 4.48 x 10-10 M
प्रश्न 7.68.
Ag2CO4 तथा AgBr का विलेयता गुणनफल स्थिरांक क्रमशः 1.1 x 10-12 तथा 5.0 x 10-13 है। उनके संतृप्त विलयन की मोलरता का अनुपात ज्ञात कीजिए।
उत्तर:
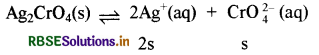
Ksp [Ag+]2 [CrO42-]
Ksp = (2s)2 (s) = 4s3
\(\mathrm{s}=\left(\frac{\mathrm{K}_{\mathrm{sp}}}{4}\right)^{\frac{1}{3}}=\left(\frac{1.1 \times 10^{-12}}{4}\right)^{\frac{1}{3}}\)
= 6.5 × 10-5 M
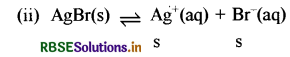
Ksp = s2, s = \(\sqrt{\mathrm{K}_{\mathrm{sp}}}\)
s = (5.0 × 10-13 )1/2 = 7.07 x 10-7 M
मौलरताओं का अनुपात = \(\frac{\left[\mathrm{Ag}_2 \mathrm{CrO}_4\right]}{[\mathrm{AgBr}]}\)
\(=\frac{6.5 \times 10^{-5}}{7.07 \times 10^{-7}}\)
= 9.19
अतः सिल्वर क्रोमेट, सिल्वर ब्रोमाइड से अधिक विलेय है।
प्रश्न 7.69.
यदि 0.002M सांद्रता वाले सोडियम आयोडेट तथा क्यूप्रिक क्लोरेट विलयन के समान आयतन को मिलाया जाए, तो क्या कॉपर आयोडेट का अवक्षेपण होगा? (कॉपर आयोडेट के लिए Ksp = 7.4 × 10-8)
उत्तर:
सोडियम आयोडेट (NalO3) तथा क्यूप्रिक क्लोरेट [Cu(CIO3)2] क्रिया करके कॉपर आयोडेट बनाते हैं।
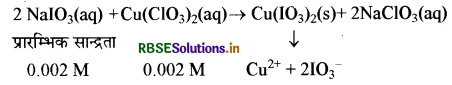
जब दोनों विलयनों के समान आयतन मिलाते हैं तो मिश्रण का आयतन दुगुना हो जाता है अतः सान्द्रता आधी हो जाएगी
[IO-3] = 0.002/2 = 0.001M
[Cu2+] = 0.002/2 = 0.001M
Cu(IO3)2 का आयनिक गुणनफल = [Cu2+] [IO3-]2
= 0.001 × (0.001)2
= 1 × 109
Cu(IO3)2 का आयनिक गुणनफल (1 x 10-9), इसके K (7.4 x 10-8) से कम है अतः कॉपर आयोडेट का अवक्षेपण नहीं होगा।
प्रश्न 7.70.
बेन्जोइक अम्ल का आयनन स्थिरांक 6.46 × 105 तथा सिल्वर बेन्जोएट का Kp 2.5 x 10 है। 3.19 pH वाले बफर विलयन में सिल्वर बेन्जोएट जल की तुलना में कितना गुना विलेय होगा?
उत्तर:
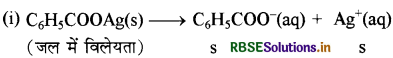
Kp = s2,
s = \(\sqrt{\mathrm{K}_{\mathrm{sp}}}\)
= (2.5 × 10-13)1/2 = 5 × 10-7 mol L-1
जल में विलेयता
= 5 x 10-7 mol L-1
(ii) बफर विलयन की pH = 3.19
pH = - log [H+]
3.19 = - log [H+]
log [H+] = - 3.19 = 4.81
[H+] = antilog 4.81 = 6.457 x 10-4 M
(antilog 0.81 = 6457)
अतः [H+] = 6.457 x 10-4 M
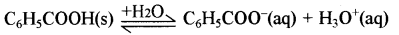
बेन्जोइक अम्ल का आयनन स्थिरांक,
\(\mathrm{K}_{\mathrm{a}}=\frac{\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{COO}^{-}\right]\left[\mathrm{H}_3 \mathrm{O}^{+}\right]}{\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{COOH}\right]}\)
\(\frac{\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{COOH}\right]}{\left[\mathrm{C}_6 \mathrm{H}_5 \mathrm{COO}^{-}\right]}=\frac{\left[\mathrm{H}_3 \mathrm{O}^{+}\right]}{\mathrm{K}_{\mathrm{a}}}=\frac{6.457 \times 10^{-4}}{6.46 \times 10^{-5}} \approx 10\)
माना बफर विलयन में सिल्वर बेन्जोएट की विलेयता = s1
[Ag+] = s1 तथा [C6H5COO] + [C6H5COOH] = s1
लगभग सारा बेन्जोएट आयन, बेंजोइक अम्ल में बदल जाता है। अत: [C6H5COO] + 10 [C6H5COO-] = s1
[C6H5COO-] = \(\frac{s^1}{11}\)
Kp = [C6H5COO-] [Ag+]
2.5 x 10-13 = \(\frac{s^1}{11} \times s^1\)
S12 = 2.75 × 10-12
s1 = 1,658 × 10-6 = 1.66 x 10-6
\(\frac{s^1}{s}=\frac{1.66 \times 10^{-6}}{5 \times 10^{-7}}\)
= 3.32
अत: सिल्वर बेन्जोएट बफर विलयन में जल की तुलना में 3.32 गुना अधिक विलेय होगा।
प्रश्न 7.71.
फैरस सल्फेट तथा सोडियम सल्फाइड के सममोलर विलयनों की अधिकतम सांद्रता बताइए जब उनके समान आयतन मिलाने पर आयरन सल्फाइड अवक्षेपित न हो। (आयरन सल्फाइड Ksp = 6.3 × 10-18 )
उत्तर:
माना फैरस सल्फेट [FeSO4 ] तथा सोडियम सल्फाइड (Na2S) की अधिकतम सान्द्रता = S mol L-1
दोनों के समान आयतन मिलाने पर सान्द्रता आधी हो जाएगी, क्योंकि आयतन दुगुना हो जाता है।
अतः
[FeSO4] = [Na2S] = S/2 M
[Fe+2] = [S-2] = S/2 M
FeSO4(aq) + Na2S(aq)- → Fe + 2S-2(s) + Na2SO4(aq)
FeS(s) = Fe2 (aq) + S2 (aq)
FeS का Kp = [Fe2+] [2]
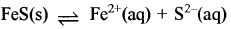
S2 = 4 × (6.3 × 10-18)
S = 5.019 × 10 = 5.02 × 109
अतः दोनों विलयनों की अधिकतम सान्द्रता = 5.02 x 10-9
लेकिन दोनों विलयनों को मिला देने पर सान्द्रता आधी रह जाती है जो कि 2.5 x 109 होगी।
प्रश्न 7.72.
1 ग्राम कैल्सियम सल्फेट को घोलने के लिए कम से कम कितने आयतन जल की आवश्यकता होगी ? (कैल्सियम सल्फेट के लिए Kp = 9.1 × 10-6)
उत्तर:
CaSO4 का Kp = s2
s = (Ksp)1/2
= (9.1 × 1 × 10-6)1/2
s = 3.016 × 103 mol L-1
CaSO4 का मोलर द्रव्यमान = 136.g mol-1
अतः g L-1 में विलेयता = 3.016 x 10-3 x 136
= 410.176 × 10-3 g
410.176 × 10-3 g CaSO4 को घोलने के लिए आवश्यक जल = 1L
अतः 1 ग्राम CaSO4 को घोलने के लिए आवश्यक जल
\(=\frac{1}{410.176 \times 10^{-3}}\)
= 2.43 L

प्रश्न 7.73.
0.1M HCl में हाइड्रोजन सल्फाइड से संतृप्त विलयन में सल्फाइड आयन की सांद्रता 10 x 10-19 M है। यदि इस विलयन का 10mL निम्नलिखित के 0.04M विलयन के 5ml में डाला जाए, तो किन विलयनों से अवक्षेप प्राप्त होगा? FeSO4 MnCl2 ZnCl2 CdCl2.
उत्तर:
किसी विद्युत अपघट्य का अवक्षेपण होने के लिए आयनिक गुणनफल का मान विलेयता गुणनफल (Ksp) से अधिक होना चाहिए। मिलाने से पहले [S-2] = 1 × 10-19 M तथा [M2] = 0.04.M
मिलाने के पश्चात् [S2] = ? [M2+] = ?
कुल आयतन = 10 + 5 = 15 mL
मिलाने के पश्चात् [S2-] MV = M2V2
= 10 × 10-19 = M2 × 15
\(\left[\mathrm{S}^{2-}\right]=\mathrm{M}_2=\frac{1 \times 10^{-19} \times 10}{15}\)
= 6.67 × 10-20 M
इसी प्रकार [M2+]
\(\frac{0.04 \times 5}{15}\)= 1.33 × 102 M.
आयनिक गुणनफल = [M2+] [S2-]
= (1.33 × 10-2) (6.67 x 10-20)
= 8.87 × 10-22
नोट: Ksp के मान पाठ्यपुस्तक से लिए गए हैं जोकि अग्र प्रकार हैं:
FeS = 6.3 × 10-18, Mns = 2.5 x 10-13,
Cds = 8.0 × 10-27
ZnS = 1.6 x 10-23
Cds के लिए आयनिक गुणनफल का मान Ksp से अधिक अतः CdCl2 का विलयन में अवक्षेपण होगा।
