RBSE Class 12 Chemistry Notes Chapter 3 वैद्युत रसायन
These comprehensive RBSE Class 12 Chemistry Notes Chapter 3 वैद्युत रसायन will give a brief overview of all the concepts.
RBSE Class 12 Chemistry Chapter 3 Notes वैद्युत रसायन
→ वैद्युत रासायनिक सेल (Electrochemical cell):
वे उपकरण या सेल या विद्युत रासायनिक साधन जिनके द्वारा हम,रासायनिक ऊर्जा को विद्युत ऊर्जा में परिवर्तित करते हैं, गैल्वैनी या वोल्टीय या विद्युत रासायनिक सेल कहलाते हैं।
→ अर्द्धसेल (Half cell):
वे सेल जिनमें ऑक्सीकरण या अपचयन अभिक्रियायें होती है, उन्हें अर्द्ध सेल कहते हैं। यदि ऑक्सीकरण की अभिक्रिया हो रही है तो इसे ऑक्सीकरण अर्द्ध-सेल और यदि अपचयन की अभिक्रिया हो रही है तो इसे अपचयन अर्द्ध-सेल कहते हैं।
→ अक्रिय विद्युत अपघट्य (Inert electrolyte):
वे विद्युत अपघट्य जो प्रक्रिया के दौरान कोई रासायनिक परिवर्तन प्रदर्शित नहीं करते हैं, अक्रिय विद्युत अपघट्य कहलाते हैं। उदाहरण-KCl, KNO3, NHANO3 आदि।
→ इलेक्ट्रोड विभव (Electrode potential):
धातु एवं धातु आयनों के विलयन के बीच उत्पन्न विद्युत विभवान्तर इलेक्ट्रोड विभव कहलाता है।
→ मानक इलेक्ट्रोड विभव (Standard electrode potential):
एक अर्द्ध-सेल में, 298K पर 1 mol L-1 सान्द्रता के धातु आयन विलयन में इलेक्ट्रोड का विभव मानक इलेक्ट्रोड विभव कहलाता है।।
→ विद्युत वाहक बल या सेल विभव (Electromotive force or cell potential):
एक विद्युत रासायनिक सेल के अवयवी दोनों इलेक्ट्रोडों के इलेक्ट्रोड विभवों के बीच अन्तर को सेल का विद्युत वाहक बल कहते हैं। इसे वोल्ट में मापते हैं। इस समय सेल में से कोई भी धारा प्रवाहित नहीं होती है।
→ विद्युत रासायनिक श्रेणी (Electrochemical series):
विभिन्न धातुओं को उनके बढ़ते या घटते हुये मानक इलेक्ट्रोड विभव के आधार पर रखने पर जो श्रेणी प्राप्त होती है उसे विद्युत रासायनिक श्रेणी कहते हैं।

→ विद्युत अपघटनी चालकत्व (Electrolytic conduction):
किसी विद्युत अपघट्य के विलयन या उसकी गलित प्रावस्था में से विद्युत प्रवाहित होने का गुण विद्युत अपघटनी चालकत्व कहलाता है।
→ चालकता (Conductivity):
यह प्रतिरोध का व्युत्क्रम होती है।
→ विशिष्ट प्रतिरोध (Specific resistance) या प्रतिरोधकता (Resistivity):
किसी विद्युत अपघटनी चालक का विशिष्ट प्रतिरोध ओम में उसका वह प्रतिरोध है जबकि चालक की लम्बाई एक सेमी. और अनुप्रस्थ परिच्छेद एक वर्ग सेमी. है अर्थात् विद्युत अपघटनी विलयन के एक घन सेमी. का प्रतिरोध उसका विशिष्ट प्रतिरोध कहलाता है।
→ विशिष्ट चालकता (Specific conductivity):
किसी विद्युत अपघटनी चालक के विशिष्ट प्रतिरोध का व्युत्क्रम उसकी विशिष्ट चालकता होती है। दूसरे शब्दों में, किसी विद्युत अपघटनी विलयन की विशिष्ट चालकता उसका वह चालकत्व है जबकि विलयन एक सेमी. दूर रखे हुये एक वर्ग सेमी. अनुप्रस्थ काट वाले दो इलेक्ट्रोडों के बीच रखा हुआ हो।
→ सेल स्थिरांक (Cell constant):
किसी सेल के दो समानान्तर इलेक्ट्रोडों के बीच की दूरी और इलेक्ट्रोड के अनुप्रस्थ काट के क्षेत्रफल का अनुपात \(\left(\frac{l}{\mathrm{~A}}\right)\) सेल स्थिरांक कहलाता है।
→ मोलर चालकता (Molar conductivity):
किसी निश्चित क्षेत्रफल वाले 1 cm की दूरी पर विद्यमान दो इलेक्ट्रोडों के मध्य उपस्थित किसी विलयन के उस आयतन की चालकता जिसमें विद्युत अपघट्य का एक ग्राम अणुभार घुला हो, उसकी मोलर चालकता कहलाती है।
→ चालक (Conductors):
वे पदार्थ जिनमें से विद्युत धारा का प्रवाह सम्भव होता है, चालक कहलाता है।
→ धात्विक चालक (Metallic conductors):
वे धात्विक पदार्थ जिनमें बिना किसी रासायनिक परिवर्तन के विद्युत धारा प्रवाहित होती है, धात्विक चालक कहलाते हैं। उदाहरण-Cu, Ag, Au आदि।
→ विद्युत अपघट्य (Electrolytes):
ऐसे पदार्थ जिनमें विद्युत धारा का प्रवाह उनकी गलित अवस्था अथवा जलीय विलयन में ही सम्भव होता है; विद्युत अपघट्य कहलाता है। उदाहरण-NaCl,
KCl, KNO3 आदि।
→ विद्युत रोधी (Insulators):
ये पदार्थ विद्युत का चालन नहीं करते हैं। उदाहरण-काँच, प्लास्टिक आदि।
→ अर्द्ध चालक (Semiconductors):
ऐसे पदार्थ जिनकी चालकता चालकों एवं विद्युतरोधियों के मध्य की होती है, अर्द्ध चालक कहलाते हैं। उदाहरण-सिलिकन (Si), जर्मेनियम (Ge) आदि।
→ अति चालक (Super conductors):
ऐसे पदार्थ जो कि शून्य प्रतिरोधकता या अनन्त चालकता वाले होते हैं, अति चालक कहलाते हैं।

→ प्रबल विद्युत अपघट्य (Strong electrolytes):
वे विद्युत अपघट्य जो विलयन में पूर्णतया आयनों में वियोजित हो जाते हैं, प्रबल विद्युत अपघट्य कहलाते हैं। उदाहरण-NaCl, KCl, HCl, KNO3 आदि।
→ दुर्बल विद्युत अपघट्य (Weak electrolytes):
वे विद्युत अपघट्य जो विलयन में पूर्णतया वियोजित नहीं होते हैं, दुर्बल विद्युत अपघट्य कहलाते हैं। उदाहरण-CH.COOH, NHOH, ZnCl3 आदि।
→ कोलराश का नियम (Kohirausch's law):
इसके अनुसार, एक वैद्युत अपघट्य की सीमान्त मोलर चालकता को उसके धनायन एवं ऋणायनों के अलग-अलग योगदान के योग के बराबर निरूपित किया जा सकता है।
→ वैद्युत अपघटनी सेल (Electrolytic cells):
ऐसे सेल जिनकी सहायता से विद्युत ऊर्जा को रासायनिक ऊर्जा में परिवर्तित किया जा सकता है। विद्युत अपघटनी सेल कहलाते हैं।
→ फैराडे का विद्युत अपघटन का प्रथम नियम (Faraday's first law of electrolysis):
इसके अनुसार, किसी भी इलेक्ट्रोड पर निक्षेपित अथवा विमुक्त किसी पदार्थ की मात्रा विद्युत अपघटनी विलयन में प्रवाहित विद्युत धारा की मात्रा के अनुक्रमानुपाती होती है।
→ फैराडे का विद्युत अपघटन का द्वितीय नियम (Faraday's second law of electrolysis):
इसके अनुसार, जब विद्युत की समान मात्रा को श्रेणीक्रम में संयोजित विभिन्न विद्युत अपघटनी विलयनों में से गुजारा जाता है, तब इलेक्ट्रोडों पर उत्पन्न पदार्थों के भार उनके रासायनिक तुल्यांक भारों के अनुक्रमानुपाती होते हैं।
→ बैटरी (Battery):
जब एक से अधिक सेलों को श्रेणीबद्ध तरीके से जोड़ते हैं तो बैटरी बनती है। वास्तव में बैटरी, गैल्वैनी सेलों की श्रेणीबद्ध तरीके से जुड़ी हुयी व्यवस्था है। बैटरी रेडॉक्स अभिक्रिया की रासायनिक ऊर्जा को विद्युत ऊर्जा में बदलती है।
→ प्राथमिक बैटरियाँ (Primary Batteries):
प्राथमिक बैटरियों में अभिक्रिया केवल एक बार होती है तथा कुछ समय के प्रयोग के बाद बैटरी निष्क्रिय हो जाती है एवं पुनः प्रयोग में नहीं लाई जा सकती है।
→ द्वितीयक बैटरियाँ (Secondary Batteries):
ये उत्क्रमणीय गैल्वैनिक सेले हैं। इनमें उच्च ऊर्जा युक्त पदार्थ शीघ्र अभिक्रिया करके विद्युत धारा व्युत्पन्न करते हैं और अक्रिय हो जाते हैं। इन पदार्थों को बाह्य स्रोतों के द्वारा पुनः सक्रिय बना लिया जाता है और पदार्थ सेल में पुनः प्रयुक्त कर लिये जाते हैं। इन सेलों को पुनः आवेशित (Recharge) किया जा सकता है। एक अच्छी एवं संचायक बैटरी कई बार डिस्चार्ज एवं चार्ज के चक्रम से गुजर सकती है।
→ ईधन सेल (Fuel cells):
ईधन सेल प्राथमिक सेल की तरह ही होती है। इसमें ईधन का दहन होता है तथा उसमें उत्पन्न रासायनिक ऊर्जा को विद्युत ऊर्जा में परिवर्तित किया जाता है। इन सेलों को इस प्रकार बनाते हैं कि इसमें ईंधन लगातार भरा जा सके जिससे कि विद्युत धारा निरन्तर प्राप्त होती रहे।
→ संक्षारण (Corrosion):
वह प्रक्रिया जिसमें धातुओं की सतह पर वायुमण्डलीय गैसें अथवा जल वाष्प के द्वारा आक्रमण से ऑक्साइड, कार्बोनेट, सल्फेट आदि बनते हैं और धीरे-धीरे धातु क्षय होने लगती है तो यह प्रक्रिया संक्षारण कहलाती है। उदाहरण-सिल्वर का बदरंग होना, कॉपर पर हरी परत का चढ़ना आदि।
→ चालकता (G) = \(\frac{1}{R}\)
यहाँ, R= प्रतिरोध

→ विशिष्ट प्रतिरोध (κ) = \(\frac{l}{A}\)G
l = लम्बाई, A = क्षेत्रफल, G = चालकता
→ सेल स्थिरांक (G*) = \(\frac{l}{A}\)
→ तुल्यांकी चालकता (Λeq) = \(\frac{1000 \times \kappa}{N}\) (ohm-1 cm-1 equiv-1) यहाँ, N = नार्मलता
→ मोलर चालकता (Λm) = \(\frac{1000 \times \kappa}{M}\) (ohm-1 cm2 mol-1) यहाँ, M = मोलरता
→ डिबाई, हकेल समीकरण,
ΛmC = Λm0 - A√C
यहाँ, C = सान्द्रता, Λm0 = शून्य सान्द्रता पर मोलर चालकता,
A = स्थिरांक।
→ वियोजन की मात्रा α = \(\frac{\Lambda_m^{\mathrm{C}}}{\Lambda_m^0}\)
यहाँ ΛmC = सान्द्रता 'C' पर आण्विक चालकता
ΛmC = शून्य सान्द्रता पर मोलर चालकता
→ कोलराउश नियम का गणितीय रूप
Λm0(AxBy) = xλ0(Ay+) + yλ0(B-x)
→ नेस्ट समीकरण के अनुसार,
Mn+ + ne- → M
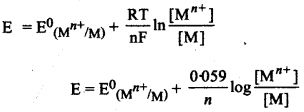
यहाँ, n = इलेक्ट्रॉनों की संख्या
→ aA + bB → cC + dD के लिये नेस्ट समीकरण
ECell = E0Cell + \(\frac{0.059}{n}\)log\(\frac{[\mathrm{A}]^a[\mathrm{~B}]^b}{[\mathrm{C}]^c[\mathrm{D}]^d}\)

→ मुक्त ऊर्जा (ΔG°) = -2.303 RTlogKC
यहाँ, R = गैस नियतांक (8.314/kmol)
T = ताप (298K)
KC = साम्य स्थिरांक
→ E0सेल = 005log KC
→ ईंधन सेल की सामर्थ्य n = \(\frac{\Delta \mathrm{G}}{\Delta \mathrm{H}}\) × 100
