RBSE Class 12 Chemistry Notes Chapter 2 विलयन
These comprehensive RBSE Class 12 Chemistry Notes Chapter 2 विलयन will give a brief overview of all the concepts.
RBSE Class 12 Chemistry Chapter 2 Notes विलयन
→ समांगी विलयन (Homogeneous solution):
जब विलयन में विलेय एवं विलायक का संघटन प्रत्येक भाग में एक समान हो अर्थात् प्रत्येक अवयव का वितरण पूर्ण विलयन में एक समान हो तो इसे समांगी विलयन कहते हैं। उदाहरण-नमक का जल में विलयन।
→ विषमांगी विलयन (Heterogeneous solution):
जब विलयन में विलेय एवं विलायक का संघटन प्रत्येक भाग में एक समान नहीं होता है तो इस प्रकार के विलयन को विषमांगी विलयन ' कहते हैं। उदाहरण-कार्बन एवं सल्फर का विलयन।
→ संतृप्त विलयन (Saturated solution):
एक निश्चित ताप पर ऐसा विलयन जो शुद्ध ठोस के साथ साम्यावस्था में हो और इस ताप पर उसमें और अधिक ठोस न घोला जा सके तो ऐसे विलयन को सन्तृप्त विलयन कहते हैं।
→ असंतृप्त विलयन (Unsaturated solution):
ऐसा विलयन जिसमें विलेय पदार्थ को उसी ताप पर और अधिक मात्रा में घोला जा सके, असंतृप्त विलयन कहलाता है।

→ अति संतृप्त विलयन (Supersaturated solution):
विलयन जिसमें एक निश्चित ताप पर उस विलयन की संतृप्त अवस्था के लिये आवश्यक मात्रा से अधिक मात्रा में विलेय पदार्थ उपस्थित हो, अति संतृप्त विलयन कहलाता है।
→ द्रव्यमान प्रतिशत (Mass percentage):
विलेय पदार्थ के भार भागों की वह संख्या जो विलयन के 100 भार भागों में उपस्थित हो विलयन की द्रव्यमान प्रतिशतता कहलाती है।
→ आयतन प्रतिशतता (Volume percentage):
विलेय पदार्थ के आयतन भागों की वह संख्या जो विलयन के 100 mL आयतन भागों में घुली हो, विलयन की आयतन/आयतन प्रतिशतता कहलाती है।
→ द्रव्यमान/आयतन प्रतिशतता (Weight/volume percentage):
विलेय पदार्थ के भार भागों की वह संख्या जो विलयन के 100 आयतन भागों में घुली हो विलयन की द्रव्यमान/आयतन प्रतिशतता कहलाती है।
→ पार्ट्स पर मिलियन (Parts per million):
जब विलेय की मात्रा अत्यन्त सूक्ष्म हो तो सान्द्रता को पार्ट्स पर मिलियन में व्यक्त किया जाता है।
→ मोल अंश (Mole fraction):
मिश्रण में किसी अवयव की मोल भिन्न मिश्रण में उस अवयव के मोल और मिश्रण के सभी अवयवों के कुल मोलों की संख्या का अनुपात होता है।
→ मोलरता (Molarity):
एक लीटर विलयन में घुले हुये विलेय के मोलों की संख्या को उस विलयन की मोलरता कहते हैं।
→ मोललता (Molality):
किसी विलयन की मोललता 1kg विलायक में उपस्थित विलेय के मोलों की संख्या होती है।
→ नार्मलता (Normality):
एक लीटर विलयन में उपस्थित विलेय पदार्थ के ग्राम तुल्यांकों की संख्या को उस विलयन की नार्मलता कहते हैं।
→ विलेयता (Solubility):
एक निश्चित ताप पर 100 g विलायक में ठोस की ग्राम में अधिकतम घुलनशील मात्रा (संतृप्त विलयन बनने तक) उसकी दिये गये विलायक में विलेयता (Solubility) कहलाती है।
→ जालक ऊर्जा (Lattice energy):
एक मोल आयनिक ठोस के आयनों को पृथक् करने के लिये आवश्यक ऊर्जा जालक ऊर्जा कहलाती है।
→ जलयोजन ऊर्जा (Hydration energy):
एक मोल ठोस में उपस्थित आयनों के जलयोजन पर मुक्त ऊर्जा, जलयोजन ऊर्जा कहलाती है।
→ हेनरी का नियम (Henry's law):
किसी गैस का वाष्प अवस्था में आंशिक दाब (p), उस विलयन में गैस के मोल अंश (x) के समानुपाती होता है।
p = KH x
यहाँ KH = हेनरी स्थिरांक, x = गैस का मोल अंश, p = गैस का दाब

→ ऐनॉक्सिया (Anoxia):
यह ऊँचाई वाली जगहों अर्थात् पहाड़ों पर रहने वाले लोगों में पायी जाने वाली एक बीमारी है। इसमें लोग स्पष्टतया सोच नहीं पाते एवं कमजोर हो जाते हैं क्योंकि पहाड़ों पर दाब कम होता है जिसके कारण रुधिर और ऊतकों में ऑक्सीजन की सन्द्रिता कम हो जाती है।
→ वाष्प दाब (Vapour pressure):
एक निश्चित ताप पर साम्यावस्था में वाष्प के अणुओं के द्वारा द्रव की सतह पर उत्पन्न किया गया दाब संतृप्त वाष्प दाब या वाष्पदाब कहलाता है।
→ वाष्पदाब में अवनमन (Lowering in vapour pressure):
यदि विलायक में कोई अवाष्पशील विलेय मिला दिया जाता है तो विलायक का वाष्पदाब कम हो जाता है इसे वाष्पदाब में अवनमन कहते हैं क्योंकि विलायक की सतह का कुछ भाग अवाष्पशील विलेय द्वारा घेर लिया जाता है।
→ रॉउल्ट का नियम (Raoult's law):
एक निश्चित ताप पर विलयन में उपस्थित एक वाष्पशील अवयव का आंशिक वाष्पदाब उस अवयव की शुद्ध अवस्था में वाष्प दाब एवं उस अवयव की मोल भिन्न के गुणनफल के बराबर होता है।
→ आदर्श विलयन (Ideal solution):
वे विलयन जो सभी तापों एवं सान्द्रता परासों पर रॉउल्ट के नियम का पालन करते हैं, आदर्श विलयन कहलाते हैं।
→ अनादर्श विलयन (Non-Ideal solution):
वे विलयन जो रॉउल्ट के नियम का पालन नहीं करते हैं, अनादर्श विलयन कहलाते हैं।
→ स्थिरक्वाथी मिश्रण (Azeotropic mixture):
ऐसा मिश्रण जो अवयवों के संघटन को प्रभावित किये बिना ही एक ताप पर आसवित होता है, स्थिरक्वाथी मि" कहलाता है। निम्नतम वाष्पदाबी स्थिरक्वायी मिश्रण (Maximum boiling azeotropes)-इसमें मिश्रण का क्वथनांक स्थिर होता है एवं वह उसके अवयवों के क्वथनांकों से अधिक होता है। उदाहरण-H2O + HCl
→ अधिकतम वाष्पदाबी स्थिरक्वायी मिश्रण (Minimum boil ing azeotropes):
इसमें मिश्रण का क्वथनांक स्थिर होता है एवं वह उसके अवयवों के क्वथनांकों से कम होता है। उदाहरण-जल + एथेनॉल
→ अणुसंख्यक गुण (Colligative properties):
विलयन के वे गुण, जो विलयन के निश्चित आयतन में उपस्थित विलेय के मोलों की संख्या या अणुओं की संख्या पर आधारित होते हैं, विलयन के अणुसंख्यक गुण कहलाते हैं।

→ क्वथनांक (Boiling point):
किसी द्रव का क्वथनांक वह ताप है जिस पर द्रव का वाष्प दाब वायुमण्डलीय दाब के बराबर होता है।
→ मोलल क्वथनांक उन्नयन स्थिरांक (Ebullioscopic constant):
किसी विलायक का मोलल क्वथनांक उन्नयन स्थिरांक इसके क्वथनांक में उन्नयन के बराबर होता है। जब एक मोल विलेय 1000 g विलायक में घोला गया हो। इसकी इकाई K kg mol-1 होती है।
→ हिमांक (Freezing point):
वह ताप जिस पर किसी द्रव की द्रव एवं ठोस अवस्थाओं का वाष्प दाब समान होता है, उसे द्रव कां हिमांक कहते हैं।
→ मोलल अवनमन स्थिरांक (Molal depression constant or cryoscopic constant):
किसी विलायक का मोलल हिमांक अवनमन स्थिरांक उसके हिमांक अवनमन के बराबर होता है जबकि इसमें एक मोल विलेय पदार्थ 1000 g विलायक में घुले हो। इसकी इकाई K kg mol-1 होती है।
→ परासरण (Osmosis):
जब निम्न सान्द्रता वाले विलयन से विलायक अर्द्धपारगम्य झिल्ली द्वारा उच्च सान्द्रता वाले विलयन की ओर प्रवाहित हो, तो इस घटना को परासरण कहते हैं।
→ अर्द्धपारगम्य झिल्ली (Semipermeable membrane):
वह झिल्ली जो जन्तु या वनस्पति मूल की हो, जो सूअर के ब्लेडर या पार्चमेन्ट की तरह प्राकृतिक रूप में मिलती हो अथवा सेलोफोन की तरह संश्लेषित प्रकृति की हो तथा जो केवल विलायक को ही अपने रन्ध्रों से गुजरने दे अर्द्धपारगम्य झिल्ली कहलाती है।
→ परासरण दाब (Osmotic pressure):
विलयन पर लगाया गया बाह्य दाब जो अर्द्धपारगम्य झिल्ली में विलायक के अणुओं का प्रवाह रोकने तथा तल में साम्य स्थापित करने के लिये आवश्यक होता है, परासरण दाब कहलाता है।
→ व्युत्क्रम परासरण या प्रतिलोम परासरण (Reverse osmosis):
यदि विलयन पर उसके परासरण दाब से अधिक दाब प्रयुक्त करें तो अर्द्धपारगम्य झिल्ली के माध्यम से विलयन से विलायक का बहाव शुद्ध विलायक की ओर होने लगता है। इस प्रक्रिया को व्युत्क्रम परासरण कहते हैं।
→ आइसोटोनिक विलयन या समपरासारी विलयन (Isotonic solutions):
वे दो विलयन जो अर्द्धपारगम्य झिल्ली से पृथक् होने पर विलायक का बहाव नहीं होने देते अर्थात् उनके परासरण दाब समान होते हैं। आइसोटोनिक विलयन कहलाते हैं। इनकी मोलर सान्द्रतायें भी समान होती हैं।
→ अतिपरासारी विलयन या हाइपरटोनिक विलयन (Hypertonic solution):
दो भिन्न परासरण दाब वाले विलयनों में से वह विलयन जिसका परासरण दाब उच्च होता है दूसरे विलयन के सापेक्ष हाइपरटोनिक विलयन कहलाता है।
→ अल्पपरासारी विलयन या हाइपोटोनिक विलयन (Hypotonic solution):
दो भिन्न परासरण दाब वाले विलयनों में वह विलयन जिसका परासरण दाब कम होता है, दूसरे के सापेक्ष हाइपोटोनिक विलयन कहलाता है।

→ वाण्टहॉफगुणांक (van'tHoff factor):
वियोजन अथवा संगुणन के कारण विलयनों के असामान्य अणुसंख्यात्मक गुणों का कारण स्पष्ट करने के लिये वाण्टहॉफ ने एक गुणांक दिया जिसे वाण्टहॉफ गुणांक (van't Hoff factor) कहते हैं।
→ द्रव्यमान % (w/W)
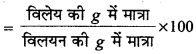
→ आयतन % (v/V) =

→ मोलरता (M)
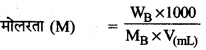
WB = विलेय का द्रव्यमान .
MB = विलेय का मोलर अणुभार
V(ml) = विलयन का आयतन
WA = विलायक का द्रव्यमान
→ मोललता
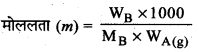
→ मोल भिन्न
xB = \(\frac{n_{\mathrm{B}}}{n_{\mathrm{A}}+n_{\mathrm{B}}}\)
nA = A के मोल
nB = B के मोल
xA = \(\frac{n_{\mathrm{A}}}{n_{\mathrm{A}}+n_{\mathrm{B}}}\)
xA = A का मोल अंश
xA + xB = 1
xB = B का मोल अंश
→ मोलरता एवं नॉर्मलता में सम्बन्ध
मोलरता × विलेय का अणुभार = नॉर्मलता × विलेय का तुल्यांकी
→ मोलरता एवं द्रव्यमान प्रतिशत में सम्बन्ध
M = \(\frac{\mathrm{P} \times d \times 10}{\mathrm{M}_{\mathrm{B}}}\)
P = द्रव्यमान प्रतिशत
d = घनत्व
MA = विलेय का मोलर द्रव्यमा
→ मोलरता एवं मोललता में सम्बन्ध
m = \(\frac{1000 \mathrm{M}}{(1000 d)-\left(\mathrm{M} \times \mathrm{M}_{\mathrm{B}}\right)}\)
जहाँ m = मोललता, M = मोलरता,
d = घनत्व, MB = विलेय का मोलर द्रव्यमान
→ मोललता एवं मोल भिन्न में सम्बन्ध
xB = \(\frac{m \times \mathrm{M}_{\mathrm{B}}}{1000+m \times \mathrm{M}_{\mathrm{B}}}\)
MB = विलेय का अणुभार
m = मोललता
xB = विलेय का मोल अंश
→ तनुता का सूत्र
M1V1 = M2V2
→ मिश्रण की मोलरता
M = \(\frac{M_1 V_1+M_2 V_2}{V_1+V_2}\)

→ मोलरता एवं मोल भिन्न में सम्बन्ध
xB = \(\frac{\mathrm{M} \times \mathrm{M}_{\mathrm{A}}}{\mathrm{M}\left(\mathrm{M}_{\mathrm{A}}-\mathrm{M}_{\mathrm{B}}\right)+1000 d}\)
d = घनत्व
MA = विलायक 'A' का अणुभार
MB = विलेय 'B' का अणुभार
M = मोलरता
xB = विलेय का मोल अंश
→ वाष्पशील विलेय के लिए रॉउल्ट का नियम
PT = PA° xA + pB° xB
PT = कुल वाष्प दाब
PA° और PB°
= क्रमशः अवयव A व B का वाष्पदाब
xA तथा xB = अवयव A व B के मोल अंश
→ अवाष्पशील विलेय के लिए रॉउल्ट का नियम
\(\frac{p_{\mathrm{A}}^0-p_{\mathrm{A}}}{p_{\mathrm{A}}^0}\) = xB
PA° = शुद्ध विलायक का वाष्प दाब
PA = विलयन का वाष्प दाब
xB = अवाष्पशील विलेय B की मोल अंश
→ क्वथनांक में उन्नयन
ΔTb = \(\frac{\mathrm{K}_b \times \mathrm{W}_{\mathrm{B}} \times 1000}{\mathrm{M}_{\mathrm{B}} \times \mathrm{W}_{\mathrm{A}}}\)
ΔTb = क्वथनांक उन्नयन
Kb = मोलल क्वथनांक उन्नयन स्थिरांक
MB = विलेय का मोलर द्रव्यमान
WB = विलेए का द्रव्यमान
WA = विलायक का द्रव्यमान g में
→ हिमांक में अवनमन
ΔTf = \(\frac{\mathrm{K}_f \times \mathrm{W}_{\mathrm{B}} \times 1000}{\mathrm{M}_{\mathrm{B}} \times \mathrm{W}_{\mathrm{A}}}\)
ΔTf = हिमांक अवनमन
Kf = मोलल हिमांक अवनमन स्थिरांक
MB = विलेय का मोलर द्रव्यमान
WB = विलेय का द्रव्यमान
WA = विलायक का द्रव्यमान g में
→ परासरण दाब
π = \(\frac{\mathrm{W}_{\mathrm{B}} \times \mathrm{R} \times \mathrm{T}}{\mathrm{M}_{\mathrm{B}} \times \mathrm{V}}\)
R = गैस नियतांक
T = ताप
V = आयतन
π = परासरण दाब
WB = विलेय का द्रव्यमान
MB = विलायक का मोलर द्रव्यमान

→ वाण्टहॉफ गुणांक से परिवर्तित अणुसंख्यक गुणधर्म
(a) \(\frac{p_{\mathrm{A}}^0-p_{\mathrm{A}}}{p_{\mathrm{A}}^0}\) = ixB
(b) ΔTb =iKbm, (i = वाण्टहॉफ गुणांक)
(c) ΔTf = iKfm
(d) πV = iCRT
→ वियोजन की मात्रा
α = \(\frac{i-1}{m-1}\)
जहाँ m = कणों की संख्या जो संगुणित हो रही है।
जहाँ m = अणुओं की संख्या
→ संगुणन की मात्रा
α = \(\frac{i-1}{\left(\frac{1}{m}\right)-1}\)
जहाँ m = कणों की संख्या जो संगुणित हो रही है।
जहाँ m = अणुओं की संख्या
