RBSE Class 12 Chemistry Notes Chapter 1 ठोस अवस्था
These comprehensive RBSE Class 12 Chemistry Notes Chapter 1 ठोस अवस्था will give a brief overview of all the concepts.
RBSE Class 12 Chemistry Chapter 1 Notes ठोस अवस्था
→ ठोस (Solid):
द्रव्य की वह अवस्था जिसमें अवयवी कण जैसे अणु, परमाणु या आयन प्रबल अन्तराण्विक आकर्षण बलों के द्वारा निविक संकलित होते हैं। ठोस अवस्था कहलाती है।
→ क्रिस्टलीय ठोस (Crystalline Solid):
इसमें अवयवी कणों की व्यवस्था दीर्घ परासी, गलनांक सुस्पष्ट एवं प्रकृति विषमदैशिक होती है।
→ अक्रिस्टलीय ठोस (Amorphous Solid):
इसमें अवयवी कणों की व्यवस्था लघु परासी, गलनांक सुस्पष्ट नहीं होता एवं प्रकृति समदैशिक होती है। यह अतिशीतित 'द्रव कहलाता है।
→ क्रिस्टल जालक (Crystal Lattice):
एक क्रिस्टलीय ठोस के अवयवी कणों (जालक बिन्दुओं) की त्रिविम में नियमित व्यवस्था (Regular arrangement) क्रिस्टल जालक या त्रिविम जालक कहलाती है।
→ जालक बिन्दु (Lattice Point):
वे बिन्दु जिन पर अवयवी कण व्यवस्थित रहते हैं जालक बिन्दु कहलाते हैं।
→ ब्रेवे जालक (Bravais Lattices):
चौदह विभिन्न प्रकार के सम्भव जालक ब्रेवे जालक कहलाते हैं।

→ एकक कोष्ठिका (Unit Cell):
जालक का वह लघु अभिलाक्षणिक भाग, जो कि पुनरावृत्ति के द्वारा जालक का निर्माण करता है, एकक कोष्ठिका कहलाता है।
→ आद्य एकक कोष्ठिका (Simple Unit Cel):
इसमें अवयवी कण केवल धन के कोनों पर व्यवस्थित होते हैं।
→ काय केन्द्रित एकक कोष्ठिका (Body Centred Unit Cell):
इसमें अवयवी कण घन के कोनों के साथ-साथ उनके अन्त:केन्द्र पर भी व्यवस्थित होते हैं।
→ फलक केन्द्रित एकक कोष्ठिका (Face centred UnitCelly):
इसमें अवयवी कण घन के कोनों के साथ-साथ फलक के केन्द्र पर व्यवस्थित होते हैं।
→ अंत्य केन्द्रित एकक कोष्ठिका (End Centred Unit Cell):
इसमें अवयवी कण घन के कोनों के साथ-साथ किन्हीं दो विपरीत फलकों के केन्द्र पर भी व्यवस्थित होते हैं।
→ संकुलन क्षमता (Packing Efficiency):
किसी भी क्रिस्टल जालक में उपस्थित कण क्रिस्टल जालक के कुल आयतन का जितना भाग घेरते हैं, उसे क्रिस्टल जालक की संकुलन क्षमता (Packing efficiency) कहा जाता है। hepया ccp या fcc की संकुलन क्षमता 74% , अन्त:केन्द्रित घनीय संरचनाओं की संकुलन क्षमता 68% तथा सरल घनीय जालक की संकुलन क्षमता 52.4% होती है।
→ अपूर्णताएँ अथवा दोष (Imperfections or Defects):
जब ठोसों की संरचनायें परिपूर्ण नहीं होती हैं तो उनमें अपूर्णताएँ अथवा दोष उपस्थित होते हैं।
→ बिन्दु दोष (Point Defect):
एक क्रिस्टलीय पदार्थ में एक बिन्दु अथवा एक परमाणु के चारों ओर की आदर्श व्यवस्था में अनियमितताएँ अथवा विचलन बिन्दु दोष (Point defect) कहलाता है।
→ स्टॉइकियोमितीय दोष (Stoichiometric defect):
इस प्रकार के बिन्दु दोष में ठोस की स्टॉइकियोमितीय पर कोई प्रभाव नहीं पड़ता है अर्थात् यहाँ क्रिस्टल में धनायन व ऋणायनों का अनुपात रासायनिक सूत्र के अनुसार ही होता है।
→ रिक्तिका दोष (Vacancy defect):
जब कुछ जालक स्थल रिक्त होते हैं तब क्रिस्टल में रिक्तिका दोष उत्पन्न होता है। इससे पदार्थ का घनत्व कम हो जाता है।
→ फ्रेंकेल दोष (Frenkel defect):
इस प्रकार के दोष में लघुतर आयन अपने वास्तविक स्थान से विस्थापित होकर अन्तराकाशी स्थल में आ जाते हैं।
→ शॉट्की दोष (Schottky defect):
इस प्रकार के दोष में समान संख्या में धनायन व ऋणायन अपने जालक बिन्दु से विस्थापित होते हैं जिससे धनत्व में कमी आ जाती है।
→ अशुद्धता दोष (Impurity defect):
इस प्रकार का दोष क्रिस्टल में अशुद्धि के कारण उत्पन्न होता है।
→ नानस्टॉइकियोमितीयोग (Non-stoichiometric defect):
इस प्रकार के दोष में धनायनों व ऋणायनों का अनुपात उन यौगिक के रासायनिक सूत्र से थोड़ा बहुत भिन्न होता है। यह धातु आधिक्य (metal excess) तथा धातु न्यून (metal deficient) प्रकार का होता
→ F-केन्द्र (F-centre):
अयुग्मित इलेक्ट्रॉनों के द्वारा भरी ऋणायनिक रिक्तिकाओं को F-केन्द्र या रंग केन्द्र कहते हैं। यह क्रिस्टल में रंग उत्पन्न करने के लिये उत्तरदायी होता है।
→ चालक (Conductors):
वे ठोस जिनमें से विद्युत धारा की अधिक मात्रा प्रवाहित होती है, चालक कहलाते हैं।
→ अचालक (Insulators):
वे ठोस जिनमें से विद्युत धारा प्रवाहित नहीं होती है, अचालक कहलाते हैं।
→ अर्द्धचालक (Semi-conductors):
वे ठोस जिनकी चालकता चालक व अचालक के मध्य की होती है, अर्द्धचालक कहलाते हैं। ये दो प्रकार के होते हैं। आन्तर अर्द्ध चालक एवं बाह्य या अपद्रव्यी अर्द्धचालक।

→ बैण्ड सिद्धान्त (Band theory):
इस सिद्धान्त के अनुसार, धातुओं के परमाणुओं के परमाण्विक कक्षक आपस में संयोजन करके आण्विक कक्षक बनाते हैं। इन आण्विक कक्षकों की ऊर्जा इतनी पास-पास होती है कि वे बैण्ड के रूप में दिखाई देते हैं।
→ निषिद्ध क्षेत्र (Forbidden zone or energy gap):
दो बैण्डों के मध्य उपस्थित रिक्त स्थल को निषिद्ध क्षेत्र कहते हैं।
→ संयोजकता बैण्ड (Valence band):
धातु परमाणु के संयोजकता कोश के परमाण्विक कक्षक आपस में मिलकर आण्विक कक्षक बनाते हैं तथा इन आण्विक कक्षकों की ऊर्जा में अन्तर अत्यन्त कम होता है, इससे ये एक बैण्ड का निर्माण करते हैं जिसे संयोजकता बैंड कहते हैं।
→ चालकता बैण्ड (Conduction Band):
पूरित संयोजकता बैण्ड से आगामी उच्च रिक्त बैण्ड चालकता बैण्ड कहलाता है।
→ अपमिश्रण (Doping):
अर्द्ध-चालकों में अशुद्धि मिलाने की विधि अपमिश्रण कहलाती है।
→ n-प्रकार के अर्द्ध-चालक (n-Type Semiconductors):
जब 14 वें वर्ग के तत्वों में 15 वें वर्ग के तत्वों जैसे-P, As, Sb इत्यादि का अपमिश्रण किया जाता है, तो n-प्रकार के अर्द्ध-चालक प्राप्त होते
→ प्रकार के अर्द्ध-चालक (p-Type Semiconductors):
जब 14वें वर्ग के तत्वों में 13 वें वर्ग के तत्वों जैसे-AI, Ga, In इत्यादि का अपमिश्रण किया जाता है, तो p-प्रकार के अर्द्ध-चालक प्राप्त होते हैं।
→ 12-16 वर्गों के यौगिक (12-16 Groups Compounds):
जब 12 वें तथा 16 वें वर्ग के तत्वों का सम्मिश्रण कर यौगिक बनाये जाते हैं तो इन्हें 12-16 वर्गों के यौगिक कहते हैं। उदाहरण-ZnS, Cds, HgTe आदि।
→ 13-15 वर्गों के यौगिक (13-15Groups Compounds):
जब 13 वें तथा 15 वें वर्ग के तत्वों का सम्मिश्रण कर यौगिक बनाये जाते हैं तो इन्हें 13-15 वर्गों के यौगिक कहते हैं। उदाहरण-InSb, AIP, GaAs आदि।
→ प्रतिचुम्बकीय पदार्थ (Diamagnetic Substances):
वे पदार्थ जो बाह्य चुम्बकीय क्षेत्र द्वारा दुर्बल रूप से प्रतिकर्षित होते हैं, प्रतिचुम्बकीय पदार्थ कहलाते हैं। इनमें अयुग्मित इलेक्ट्रॉन नहीं होते हैं। उदाहरण-TiO2, NaCl, V2O3 आदि।
→ अनुचुम्बकीय पदार्थ (Paramagnetic Substances):
वे पदार्थ जो बाह्य चुम्बकीय क्षेत्र द्वारा दुर्बल रूप से आकर्षित होते हैं, अनुचुम्बकीय पदार्थ कहलाते हैं। इनमें अयुग्मित इलेक्ट्रॉन उपस्थित होते हैं। उदाहरण-TiO, Cuo, Vo, आदि।
→ लौहचुम्बकीय पदार्थ (Ferromagnetic Substances):
वे पदार्थ जो बाह्य चुम्बकीय क्षेत्र द्वारा प्रबलता से आकर्षित होते हैं एवं चुम्बकीय क्षेत्र की अनुपस्थिति में भी स्थायी चुम्बकत्व प्रदर्शित करते हैं, लौहचुम्बकीय पदार्थ कहलाते हैं। उदाहरण-CrO2, Ni, Co आदि।
→ फेरीचुम्बकत्व पदार्थ (Ferrimagnetic Substances):
वे पदार्थ जिनमें अयुग्मित इलेक्ट्रॉनों की उपस्थिति के कारण प्रबल चुम्बकत्व की अपेक्षा की जाती है परन्तु वास्तव में उनमें चुम्बकत्व कम ही होता है लघु लौहचुम्बकीय पदार्थ कहलाते हैं। उदाहरण-Fe3O MgFe2O4 आदि।

→ प्रति लौहचुम्बकीय पदार्थ (Anti Ferromagnetic Substances):
इस प्रकार के पदार्थों में अयुग्मित इलेक्ट्रानों की उपस्थिति के कारण अचुम्बकीय या लौहचुम्बकीय होने की परिकल्पना की जाती है परन्तु इनमें चुम्बकीय आघूर्ण का मान शून्य होता है। उदाहरण-MnO, MnO4, V2O3 आदि।
→ घनत्व की गणना, जहाँ, Z = एकक कोष्ठिका में उपस्थित परमाणुओं की संख्या
d = \(\frac{\mathrm{ZM}}{(a)^3 \cdot \mathrm{N}_{\mathrm{A}}}\)
d = घनत्व
M = मोलर द्रव्यमान
a = कोर की लम्बाई
NA = आवोगाद्रो संख्या (6.022 × 1023)
→ एकक कोष्ठिका के विभिन्न पैरामीटर एवं महत्वपूर्ण सूत्र
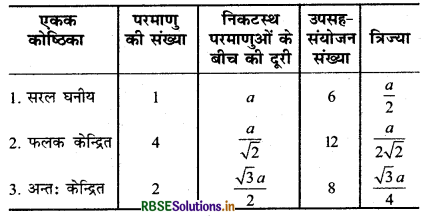
जहाँ a = कोर की लम्बाई।
→ संकुलन क्षमता- % संकुलन क्षमता एकक कोष्ठिका में गोलों द्वारा अध्यासित आयतन ।
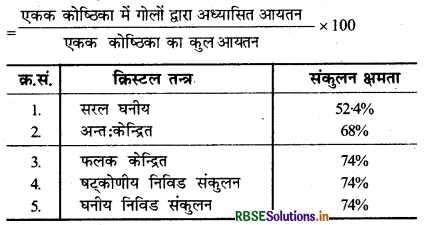
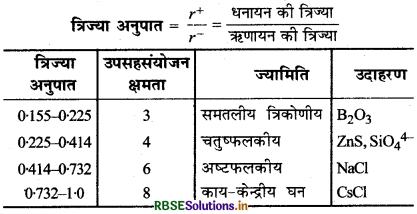
→ त्रिज्या अनुपात