RBSE Class 11 Chemistry Important Questions Chapter 10 s-ब्लॉक तत्त्व
Rajasthan Board RBSE Class 11 Chemistry Important Questions Chapter 10 s-ब्लॉक तत्त्व Important Questions and Answers.
RBSE Class 11 Chemistry Chapter 10 Important Questions s-ब्लॉक तत्त्व
बहुचयनात्मक प्रश्न (Multiple Choice Questions):
प्रश्न 1.
क्षार धातुओं का परमाणु क्रमांक बढ़ने पर:
(अ) आयनन विभव बढ़ता है
(ब) विद्युतऋणता बढ़ती है
(स) आयनिक त्रिज्या बढ़ती है
(द) अपचायक गुण कम होता है।
उत्तर:
(स) आयनिक त्रिज्या बढ़ती है
प्रश्न 2.
कम आयनन एन्थैल्पी के परिणामस्वरूप क्षार धातुएँ निम्नलिखित गुण दर्शाती हैं:
(अ) अच्छे ऑक्सीकारक
(ब) अच्छे अपचायक
(स) दुर्बल ऑक्सीकारक
(द) दुर्बल अपचायक तथा उपचायक
उत्तर:
(ब) अच्छे अपचायक

प्रश्न 3.
कार्बनिक विलायकों में अधिक विलेय क्लोराइड है:
(अ) NaCl
(ब) CaCl2
(स) LiCl
(द) KCl
उत्तर:
(स) LiCl
प्रश्न 4.
क्षार धातु वर्ग का कौनसा सदस्य धातु नहीं है?
(अ) H
(ब) Li
(स) Na
(द) Fr
उत्तर:
(अ) H
प्रश्न 5.
निम्नलिखित में प्रबलतम अपचायक धातु कौनसा है?
(अ) Li
(ब) Na
(स) Rb
(द) Cs
उत्तर:
(अ) Li
प्रश्न 6.
वह तत्व जो ज्वाला परीक्षण करने पर बैंगनी रंग की ज्वाला देता है, वह है:
(अ) Na
(ब) K
(स) Ca
(द) Sr
उत्तर:
(ब) K
प्रश्न 7.
क्षार धातुओं को जब द्रव NH3 में घोला जाता है तो विलयन का रंग होता है:
(अ) नीला
(ब) हरा
(स) पीला
(द) लाल
उत्तर:
(ब) हरा
प्रश्न 8.
निम्नलिखित में से तत्वों का कौनसा युग्म विकर्ण संबंध प्रदर्शित करता है?
(अ) Na तथा Ca
(ब) B तथा Al
(स) Be तथा Al
(द) K तथा Sr
उत्तर:
(स) Be तथा Al
प्रश्न 9.
निम्नलिखित में से आर्द्रताग्राही क्लोराइड है:
(अ) NaCl
(ब) KCL
(स) MgCl2
(द) BaCl2
उत्तर:
(स) MgCl2
प्रश्न 10.
प्रकाश वैद्युत सेल में प्रयुक्त धातु है:
(अ) Li
(ब) Mg
(स) Rb
(द) Cs
उत्तर:
(द) Cs
प्रश्न 11.
क्षार धातुओं के कार्बोनेटों के तापीय स्थायित्व का घटता क्रम
(अ) Li2CO3 > Na2CO3 > K2CO3
(ब) Na2CO3 > K2CO3 < Li2CO3
(स) K2CO3 > Na2CO3 > Li2CO3
(द) K2CO3 > Li2CO3 > Na2CO3
उत्तर:
(स) K2CO3 > Na2CO3 > Li2CO3

प्रश्न 12.
क्षार धातुओं की अपचायक सामर्थ्य का सही क्रम है:
(अ) Li> Cs > Rb > K > Na
(ब) Na > Cs > Rb > K > Li
(स) K > Cs > Rb > Na > Li
(द) Rb > Cs > K > Na > Li
उत्तर:
(अ) Li> Cs > Rb > K > Na
प्रश्न 13.
क्षार धातु हाइड्रॉक्साइडों की क्षारीय प्रकृति का बढ़ता क्रम है:
(अ) LiOH < NaOH < KOH < RbOH
(ब) NaOH < KOH < RbOH < LiOH
(स) KOH < RbOH < LiOH < NaOH
(द) RbOH < LiOH < NaOH < KOH
उत्तर:
(अ) LiOH < NaOH < KOH < RbOH
प्रश्न 14.
धोने के सोडे ( धावन सोडा) का सूत्र है:
(अ) Na2CO3
(ब) NaHCO3
(स) Na2CO3. H2O
(द) Na2CO3.10H2O
उत्तर:
(द) Na2CO3.10H2O
प्रश्न 15.
'कार्नेलाइट' का सूत्र है:
(अ) KCl
(ब) KCl. MgCl2. 2H2O
(स) KCl. MgCl2 6H2O
(द) K2SO4. MgSO4
उत्तर:
(स) KCl. MgCl2 6H2O
प्रश्न 16.
संगमरमर पत्थर का प्रमुख अवयव है:
(अ) CaCO3
(ब) CaCO3. 2H2O
(स) CaCl2.2H2O
(द) CaSO4
उत्तर:
(अ) CaCO3
प्रश्न 17.
'जिप्सम' का सूत्र है:
(अ) CaSO4
(ब) CaSO4. 2H2O
(स) CaCl2
(द) Ca(OH)2
उत्तर:
(ब) CaSO4. 2H2O
प्रश्न 18.
'प्लास्टर ऑफ पेरिस' का सूत्र है:
(अ) CaSO4
(ब) (CaSO4)2. H2O
(स) Ca(NO3)2
(द) Ca3 (PO4)3
उत्तर:
(ब) (CaSO4)2. H2O

प्रश्न 19.
s - ब्लॉक के तत्वों का सामान्य इलेक्ट्रॉनिक विन्यास है:
(अ) ns2 तथा ns2
(ब) ns2 nd1-6
(स) (n-1)dl-10 ns 2
(द) (n - 2)f1-14 (n-1)d-1ns2
उत्तर:
(द) (n - 2)f1-14 (n-1)d-1ns2
प्रश्न 20.
निम्नलिखित में से कौनसे तत्त्व की आयनन एन्थैल्पी न्यूनतम है?
(अ) Li
(ब) Rb
(स) K
(द) Cs
उत्तर:
(द) Cs
प्रश्न 21.
चिली साल्टपीटर है:
(अ) NaNO3
(ब) KNO3
(स) Na2 SO4
(द) Na2S2O3
उत्तर:
(अ) NaNO3
प्रश्न 22.
क्लोरोफिल में उपस्थित धातु है:
(अ) Li
(ब) Na+
(स) Mg
(द) Fr+
उत्तर:
(स) Mg
प्रश्न 23.
निम्नलिखित में सबसे छोटा धनायन है:
(अ) Li+
(ब) Be
(स) K+
(द) Ca
उत्तर:
(अ) Li+
प्रश्न 24.
निम्नलिखित में प्रबलतम क्षारीय हाइड्रॉक्साइड है:
(अ) Mg (OH)2
(ब) Be (OH) 2
(स) Ca(OH)2
(द) Ba(OH)2
उत्तर:
(द) Ba(OH)2

प्रश्न 25.
इंडियन साल्टपीटर का सूत्र है:
(अ) KNO3
(ब) NaCl
(स) NaNO3
(द) Na2CO3
उत्तर:
(अ) KNO3
रिक्त स्थान वाले प्रश्न (Fill in the blanks):
प्रश्न 1.
वर्ग 1 में नीचे जाने पर सामान्यतः घनत्व का मान ......................... है।
उत्तर:
बढ़ता
प्रश्न 2.
क्षारीय मृदा धातु ............................ ऑक्सीकरण अवस्था दर्शाते हैं।
उत्तर:
+2
प्रश्न 3.
........................... को प्रकाश विद्युत सेल में प्रयुक्त किया जाता है
उत्तर:
सीजियम
प्रश्न 4.
Mg(OH)2 का क्षारीय गुण, Ca(OH)2 के क्षारीय गुण से .................... होता है।
उत्तर:
कम

प्रश्न 5.
पोटैशियम ज्वाला को ............................... रंग प्रदान करता है।
उत्तर:
बैंगनी
प्रश्न 6.
प्रथम वर्ग में नीचे जाने पर कार्बोनेटों का स्थायित्व .............................. है।
उत्तर:
बढ़ता
प्रश्न 7.
सामान्य s - ब्लॉक के तत्व द्रव अमोनिया में ............................... हैं।
उत्तर:
विलेय
प्रश्न 8.
CaSO4 .7H2O को भी .......................... कहते हैं।
उत्तर:
प्लास्टर ऑफ पेरिस
प्रश्न 9.
क्षार धातुओं के गलनांक तथा क्वथनांक .......................... होते हैं।
उत्तर:
कम।
निम्नलिखित में से सत्य एवं असत्य कथन छाँटिए (True and False Statement):
प्रश्न 1.
पोटैशियम का घनत्व, सोडियम के घनत्व से कम होता है।
उत्तर:
सत्य
प्रश्न 2.
क्षार धातुएँ कठोर होती हैं।
उत्तर:
असत्य
प्रश्न 3.
क्षारीय मृदा धातुओं का बाह्यतम इलेक्ट्रॉनिक विन्यास ns होत है।
उत्तर:
असत्य

प्रश्न 4.
जलयोजन ऊर्जा, आयनिक त्रिज्या के व्युत्क्रमानुपाती होती है।
उत्तर:
सत्य
प्रश्न 5.
वर्ग में नीचे जाने पर धात्विक गुण घटता है।
उत्तर:
असत्य
प्रश्न 6.
क्षार धातु आयन प्रतिचुम्बकीय होते हैं।
उत्तर:
सत्य
प्रश्न 7.
Na2O2 एक सुपर ऑक्साइड है।
उत्तर:
असत्य
प्रश्न 8.
KOH का उपयोग CO2 के अवशोषक के रूप में किया जात है।
उत्तर:
सत्य
मिलान करने वाले प्रश्न (Matching type Questions):
सूची A तथा सूची B का मिलान कीजिए तथा सही कूट (Code) का चयन कीजिए:
प्रश्न 1.
|
सूची A |
सूची B |
|
(1) विकर्ण सम्बन्ध |
(a) NaOH |
|
(2) साल्वे विधि |
(b) Li तथा Mg |
|
(3) कास्टिक सोडा |
(c) सोडियम कार्बोनेट का निर्माण |
|
(4) बेकिंग सोडा |
(d) NaHCO3 |
उत्तर:
|
सूची A |
सूची B |
|
(1) विकर्ण सम्बन्ध |
(b) Li तथा Mg |
|
(2) साल्वे विधि |
(c) सोडियम कार्बोनेट का निर्माण |
|
(3) कास्टिक सोडा |
(a) NaOH |
|
(4) बेकिंग सोडा |
(d) NaHCO3 |

प्रश्न 2.
|
सूची A |
सूची B |
|
(1) पेट की अम्लता कम करने वाला पदार्थ |
(a) लीथियम |
|
(2) उच्च ऋणात्मक मानक इलेक्ट्रॉड विभव |
(b) Na2CO3 |
|
(3) क्षारीय विलयन |
(c) Ra (रेडियम) |
|
(4) रेडियोधर्मी तत्व |
(d) प्रति अम्ल |
उत्तर:
|
सूची A |
सूची B |
|
(1) पेट की अम्लता कम करने वाला पदार्थ |
(d) प्रति अम्ल |
|
(2) उच्च ऋणात्मक मानक इलेक्ट्रॉड विभव |
(a) लीथियम |
|
(3) क्षारीय विलयन |
(b) Na2CO3 |
|
(4) रेडियोधर्मी तत्व |
(c) Ra (रेडियम) |
प्रश्न 3.
|
सूची A |
सूची B |
|
(1) कैल्सियम का ज्वाला परीक्षण |
(a) MCl2 |
|
(2) जलयोजन एन्थैल्पी |
(b) Mg3N2 |
|
(3) Mg की वायु के साथ क्रिया |
(c) ईंट जैसा लाल रंग |
|
(4) क्षारीय मृदा धातुओं की HCl से क्रिया |
(d) Mg+2 > Sr+2 |
उत्तर:
|
सूची A |
सूची B |
|
(1) कैल्सियम का ज्वाला परीक्षण |
(c) ईंट जैसा लाल रंग |
|
(2) जलयोजन एन्थैल्पी |
(d) Mg+2 > Sr+2 |
|
(3) Mg की वायु के साथ क्रिया |
(a) MCl2 |
|
(4) क्षारीय मृदा धातुओं की HCl से क्रिया |
(b) Mg3N2 |
प्रश्न 4.
|
सूची A |
सूची B |
|
(1) Mg - Al मिश्र धातु |
(a) Mg(OH)2 का जल में निलम्बन |
|
(2) मिल्क ऑफ मैग्नीशियम |
(b) Be(OH)2 |
|
(3) रेडियम के लवण |
(c) वायुयानों का निर्माण |
|
(4) उभयधर्मी गुण |
(d) विकिरण चिकित्सा |
उत्तर:
|
सूची A |
सूची B |
|
(1) Mg - Al मिश्र धातु |
(c) वायुयानों का निर्माण |
|
(2) मिल्क ऑफ मैग्नीशियम |
(a) Mg(OH)2 का जल में निलम्बन |
|
(3) रेडियम के लवण |
(d) विकिरण चिकित्सा |
|
(4) उभयधर्मी गुण |
(b) Be(OH)2 |
प्रश्न 5.
|
सूची A |
सूची B |
|
(1) लूइस अम्ल |
(a) मृततापित प्लास्टर |
|
(2) CaC2 + H2O |
(b) AlCl3 |
|
(3) संगमरमर |
(c) C2H2 |
|
(4) शुष्क कैल्सियम सल्फेट |
(d) CaCO3 |
उत्तर:
|
सूची A |
सूची B |
|
(1) लूइस अम्ल |
(b) AlCl3 |
|
(2) CaC2 + H2O |
(c) C2H2 |
|
(3) संगमरमर |
(d) CaCO3 |
|
(4) शुष्क कैल्सियम सल्फेट |
(a) मृततापित प्लास्टर |

प्रश्न 7.
|
सूची A |
सूची B |
|
(1) मैग्नीशियम |
(a) Ca(HCO3)2 |
|
(2) जिप्सम |
(b) CaSiO3 |
|
(3) रंगहीन विलयन |
(c) क्लोरोफिल |
|
(4) कैल्सियम सिलिकेट |
(d) CaSO4 . 2H2O |
उत्तर:
|
सूची A |
सूची B |
|
(1) मैग्नीशियम |
(c) क्लोरोफिल |
|
(2) जिप्सम |
(d) CaSO4 . 2H2O |
|
(3) रंगहीन विलयन |
(a) Ca(HCO3)2 |
|
(4) कैल्सियम सिलिकेट |
(b) CaSiO3 |
प्रश्न 8.
|
सूची A |
सूची B |
|
(1) प्लास्टर ऑफ पेरिस |
(a) KCl. MgCl2 . 6H2O |
|
(2) चिली साल्ट पीटर |
(b) दन्त चिकित्सा |
|
(3) कार्नेलाइट |
(c) Na2CO3 |
|
(4) जल की स्थायी कठोरता दूर करना |
(d) NaNO3 |
उत्तर:
|
सूची A |
सूची B |
|
(1) प्लास्टर ऑफ पेरिस |
(b) दन्त चिकित्सा |
|
(2) चिली साल्ट पीटर |
(d) NaNO3 |
|
(3) कार्नेलाइट |
(a) KCl. MgCl2 . 6H2O |
|
(4) जल की स्थायी कठोरता दूर करना |
(c) Na2CO3 |
अतिलघूत्तरात्मक प्रश्न (Very Short Answer Type Questions):
प्रश्न 1.
उस क्षार धातु का नाम बताइए जो जलयोजित लवण बनाती है।
उत्तर:
लीथियम (Li)।
प्रश्न 2.
Na धातु को किस द्रव में रखा जाता है?
उत्तर:
Na को मिट्टी के तेल ( किरोसिन) में रखा जाता है, क्योंकि यह बहुत क्रियाशील होता है।
प्रश्न 3.
जल की स्थायी कठोरता दूर करने के लिए सोडियम का कौनसा लवण प्रयुक्त किया जाता है?
उत्तर:
Na2CO3 द्वारा जल की स्थायी कठोरता दूर की जाती है।

प्रश्न 4.
CO2 गैस को सोखने का गुण किस यौगिक में पाया जाता है?
उत्तर:
NaOH, CO2 गैस को सोख लेता है।
प्रश्न 5.
क्षार धातुओं के घनत्व का बढ़ता क्रम बताइए।
उत्तर:
Li< K< Na < Rb < Cs
प्रश्न 6.
सुपर ऑक्साइड बनाने वाली क्षार धातु का नाम बताइए।
उत्तर:
K, Rb तथा Cs सुपर ऑक्साइड बनाते हैं।
प्रश्न 7.
बेकिंग सोडा अथवा मीठा सोडा का सूत्र बताइए।
उत्तर:
NaHCO3 ( सोडियम हाइड्रोजन - कार्बोनेट) को बेकिंग सोडा कहते हैं।
प्रश्न 8.
धातु - अमोनिया विलयन विद्युत का सुचालक क्यों होता है?
उत्तर:
मुक्त इलेक्ट्रॉनों के कारण धातु अमोनिया विलयन विद्युत का सुचालक होता है।
प्रश्न 9.
Na+ का एक जैविक महत्व दीजिए।
उत्तर:
Na+ तन्त्रिका आवेग संचरण में भाग लेता है।
प्रश्न 10.
प्रथम वर्ग में सबसे कठोर धातु कौनसी होती है?
उत्तर:
लीथियम।
प्रश्न 11.
कौनसी क्षार धातु को प्रकाश विद्युत सेल के इलेक्ट्रॉड बनाने में प्रयुक्त किया जाता है?
उत्तर:
सीजियम (Cs)।
प्रश्न 12.
वे प्रोटॉनदाता यौगिक कौनसे होते हैं जिनसे क्षार धातुएँ आसानी से अभिक्रिया करती हैं?
उत्तर:
क्षार धातुएँ ऐल्कोहॉल, अमोनिया तथा एसिटिलीन (HC = CH) इत्यादि प्रोटॉनदाता यौगिकों से आसानी से अभिक्रिया करती हैं।
प्रश्न 13.
क्षार धातु हैलाइडों के गलनांक का सामान्य क्रम बताइए।
उत्तर:
MF > MC1 > MBr > MI
प्रश्न 14.
लीथियम के हैलाइडों की जल में विलेयता का बढ़ता क्रम क्या होता है?
उत्तर:
LiF < LiC1 < LiBr < Lil
प्रश्न 15.
क्षार धातु फ्लुओराइडों की जल में विलेयता का क्रम लिखिए।
उत्तर:
LiF < NaF < KF < RbF < CsF

प्रश्न 16.
Be, Al के साथ गुणों में समानताएँ क्यों दर्शाता है?
उत्तर:
विकर्ण संबंध के कारण Be, Al के साथ गुणों में समानताएँ दर्शाता है।
प्रश्न 17.
बिना बुझा चूना का सूत्र बताइए।
उत्तर:
CaO को बिना बुझा चूना कहते हैं।
प्रश्न 18.
क्षार धातुएँ +2 ऑक्सीकरण अवस्था क्यों नहीं दर्शाती हैं ?
उत्तर:
क्षार धातुएँ एक इलेक्ट्रॉन त्यागकर स्थायी उत्कृष्ट गैस विन्यास प्राप्त कर लेती हैं, जिसमें से इलेक्ट्रॉन निकलना मुश्किल होता है। अतः ये +2 ऑक्सीकरण अवस्था नहीं दर्शातीं।
प्रश्न 19.
मृत तापित प्लास्टर (Dead burnst Plaster) किसे कहते हैं?
उत्तर:
निर्जल CaSO4 को मृत तापित प्लास्टर कहते हैं।
प्रश्न 20.
Ca(OH)2 तथा Ba(OH)2 में से अधिक प्रबल क्षार कौनसा है?
उत्तर:
Ba(OH)2
लघूत्तरात्मक प्रश्न (Short Answer Type Questions ):
प्रश्न 1.
(a) सोडियम को मिट्टी के तेल में क्यों रखा जाता है?
(b) क्षार धातुएँ द्विधनात्मक आयन नहीं बनाती हैं। क्यों?
उत्तर:
(a) सोडियम एक क्रियाशील धातु है अतः यह वायु से क्रिया करके ऑक्साइड तथा परॉक्साइड बनाती है तथा जल से क्रिया करके हाइड्रॉक्साइड्स बनाती है। मिट्टी का तेल हाइड्रोकार्बन का मिश्रण होता है जो कि सोडियम से क्रिया नहीं करता है, अतः इसे मिट्टी के तेल में रखा जाता है।
(b) क्षार धातुओं के बाह्यतम कोश में एक इलेक्ट्रॉन पाया जाता है जिसे त्यागकर ये स्थायी उत्कृष्ट गैस विन्यास प्राप्त कर लेती हैं जिसमें से इलेक्ट्रॉन निकालना मुश्किल होता है। अतः क्षार धातुएँ द्वि- धनात्मक आयन नहीं बनातीं तथा ये केवल + 1 ऑक्सीकरण अवस्था ही दर्शाती हैं।
प्रश्न 2.
सीजियम का उपयोग प्रकाश विद्युत सेल में किया जाता है। क्यों ?
उत्तर:
सीजियम का आकार बड़ा होता है, अतः इसमें इलेक्ट्रॉन ढीले बँधे होते हैं। इसलिए इसका आयनन विभव भी बहुत कम होता है। यही कारण है कि थोड़ी-सी प्रकाशीय ऊर्जा से इसके इलेक्ट्रॉन बाहर निकल जाते हैं अर्थात् इसमें प्रकाश विद्युत प्रभाव आसानी से होता है अतः इसका उपयोग प्रकाश विद्युत सेल में किया जाता है।

प्रश्न 3.
LiCl सहसंयोजक होता है जबकि NaCl आयनिक, क्यों?
उत्तर:
LiCl के छोटे आकार के कारण यह Cl का ध्रुवण अधिक करता है। अतः फायान के नियमानुसार इसमें सहसंयोजक गुण आ जाता है जबकि Na+ का आकार बड़ा होने के कारण यह Cl का ध्रुवण नहीं करता है, अत: NaCl आयनिक है।
प्रश्न 4.
Na2CO3 की तनु HCl, तनु H2SO4 तथा जलीय CO2 के साथ अभिक्रियाएँ दीजिए।
उत्तर:
Na2CO3 की तनु HCl के साथ क्रिया से NaCl, H2O तथा CO2 बनती है।
यह H2SO4 से निम्न प्रकार क्रिया करता है:
Na2CO3 + H2SO4 (तनु) → Na2SO4 + H2O + CO2
यह जलीय CO2 से क्रिया करके सोडियम हाइड्रोजन कार्बोनेट बनाता है।
Na2CO3 + H2O + CO2 → 2NaHCO3 (सोडियम हाइड्रोजन कार्बोनेट)
प्रश्न 5.
क्षार धातु आयन रंगहीन तथा प्रतिचुम्बकीय होते हैं,
उत्तर:
क्षार धातु आयनों में उत्कृष्ट गैस विन्यास होने के कारण इनमें सभी इलेक्ट्रॉन युग्मित होते हैं अतः ये रंगहीन तथा प्रतिचुम्बकीय होते हैं।
प्रश्न 6.
(a) CsI जल में कम विलेय होता है, क्यों?
(b) मैग्नीशियम के फीते को नाइट्रोजन के साथ गरम करने से प्राप्त यौगिक की जल से क्रिया कराने पर कौनसी गैस प्राप्त होती है?
उत्तर:
(a) CsI की जल में विलेयता कम होती है क्योंकि Cs+ तथा I के बड़े आकार के कारण जलयोजन ऊर्जा का मान कम होता है।
(b) अमोनिया तथा अभिक्रियाओं के समीकरण निम्नलिखित हैं-
6Mg + 2N2 → 2Mg3N2
Mg3N2 + 6H2O → 2NH3 + 3Mg(OH)2
प्रश्न 7.
NaCl के जलीय विलयन के विद्युत अपघटन से सोडियम धातु प्राप्त नहीं की जा सकती है। क्यों?
उत्तर:
NaCl के जलीय विलयन के विद्युत अपघटन से कैथोड पर सोडियम प्राप्त होता है लेकिन इसकी क्रियाशीलता बहुत अधिक होने के कारण यह तुरन्त जल से क्रिया करके NaOH तथा H2 देता है अतः NaCl के जलीय विलयन के विद्युत अपघटन से सोडियम धातु प्राप्त नहीं की जा सकती है।
प्रश्न 8.
बेकिंग सोडा को पेस्ट्री केक इत्यादि में मिलाया जाता है, क्यों?
उत्तर:
बेकिंग सोडा को पेस्ट्री केक इत्यादि में इसलिए मिलाया जाता है क्योंकि यह गरम होने पर विघटित होकर CO2 गैस के बुलबुले देता है जिससे पेस्ट्री, केक में छोटे-छोटे छिद्र हो जाते हैं जिससे ये हल्की तथा परिफुल्लित (fluffy) हो जाती हैं।
प्रश्न 9.
क्षारीय मृदा धातुओं के घनत्व में नियमितता नहीं होती है, क्यों?
उत्तर:
क्षारीय मृदा धातुओं में Be से Ca तक घनत्व कुछ कम होता है, इसके पश्चात् घनत्व बढ़ता है। इसका कारण इनकी क्रिस्टल संरचना में अन्तर है। अतः क्षारीय मृदा धातुओं में घनत्व का क्रम इस प्रकार होता है
Ca < Mg < Be < Sr < Ba
प्रश्न 10.
(a) BeH2 को बनाने की विधि बताइए।
(b) क्षारीय मृदा धातुओं के हाइड्राइडों की जल से अभिक्रिया कराने पर क्या होता है?
(c) वर्ग 2 के तत्त्वों के हाइड्राइडों के तापीय स्थायित्व का क्रम बताइए।
उत्तर:
(a) BeCl2 की LiAIH के साथ अभिक्रिया करवाने पर BeH2 प्राप्त होता है।
2BeCl2 + LiAlH4 → 2BeH2 + LiCl + AlCl3
(b) क्षारीय मृदा धातुओं के हाइड्राइडों की जल से क्रिया कराने पर संगत धातु हाइड्रॉक्साइड तथा हाइड्रोजन बनती है।
MH2 + 2H2O → M(OH)2 + 2H2
(c) वर्ग 2 के तत्वों के हाइड्राइडों के तापीय स्थायित्व का क्रम निम्नलिखित है
BeH2 > MgH2 > CaH > SrH2 > BaH2
प्रश्न 11.
प्लास्टर ऑफ पेरिस क्या होता है? इसके गुण भी बताइए।
उत्तर:
प्लास्टर ऑफ पेरिस कैल्सियम सल्फेट का अर्धहाइड्रेट (Hemihydrate) होता है। CaSO4 1/2H2O इसे जिम्सम (CaSO4. 2H2O) को 393K पर गरम करके बनाया जाता है।
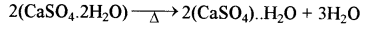
393 K से उच्च ताप पर गर्म करने पर इसमें क्रिस्टलन जल नहीं बचता है तथा शुष्क कैल्सियम सल्फेट (CaSO4) प्राप्त होता है। इसे 'मृत तापित प्लास्टर' (Dead Burnt Plaster) कहते हैं। इसमें जल के साथ जमने की विशेष प्रकृति होती है पर्याप्त मात्रा में जल मिलाने पर यह एक प्लास्टिक जैसा द्रव्य बनाता है, जो 5 से 15 मिनट में जमकर कठोर तथा ठोस हो जाता है।
प्रश्न 12.
क्षार धातुओं तथा क्षारीय मृदा धातुओं में समानताएँ
उत्तर:
क्षार धातुओं तथा क्षारीय मृदा धातुओं में निम्नलिखित सक्षारतुएँ होता है।
|
क्षार धातुएँ [ वर्ग (1) के तत्व ] |
क्षारीय मृदा धातुएँ [ वर्ग (2) के तत्व ] |
|
1. इनमें संयोजकता कोश -s- कक्षक है। |
समान रूप से संयोजकता कोश - s- कक्षक है। |
|
2. ये विद्युत - धनी तत्व हैं। |
ये भी विद्युत - धनी तत्व हैं । |
|
3. धात्विक तत्व हैं। |
धात्विक तत्व हैं। |
|
4. प्रबल अपचायक हैं। |
प्रबल अपचायक हैं । |
|
5. अंतिम सदस्य रेडियोधर्मी होता है। |
इनका भी अंतिम सदस्य रेडियोधर्मी होता है । |
|
6. प्रथम तत्व (Li) का व्यवहार वर्ग के अन्य सदस्यों से भिन्न होता है |
इनमें भी प्रथम सदस्य (Be) वर्ग के अन्य सदस्यों से भिन्न व्यवहार दर्शाता है तथा विकर्ण सम्बन्ध दर्शाता है। |
|
7. तथा यह विकर्ण सम्बन्ध दर्शाता है। |
ये भी ज्वाला को रंग प्रदान करते हैं। |
|
8. ज्वाला को रंग प्रदान करते हैं। |
इनका भी मानक अपचयन विभव उच्च ऋणात्मक होता है। |
|
9. मानक अपचयन विभव उच्च ऋणात्मक होता है। |
इनका भी मानक अपचयन विभव उच्च ऋणात्मक होता है। |

प्रश्न 13.
वर्ग 1 तथा वर्ग 2 के तत्त्वों में असमानताएँ बताइए
उत्तर:
वर्ग 1 तथा वर्ग 2 के तत्त्वों में अग्रलिखित असमानताएँ होती है।
|
गुण |
वर्ग 1 के तत्त्व ( क्षार धातु ) |
वर्ग 2 के तत्त्व (क्षारीय मृदा धातु ) |
|
1. ऑक्सीकरण अवस्था |
+ 1 |
+2 |
|
2. गलनांक |
कम होता है । |
क्षार धातुओं से अधिक होता है। |
|
3. विद्युत धनात्मक प्रकृति |
प्रबल धन- विद्युती हैं। |
क्षार धातुओं से कम विद्युत धनी हैं। |
|
4. जल के साथ अभिक्रिया |
अधिक तीव्र गति से क्रिया होती है। |
क्षार धातुओं की अपेक्षा धीमी गति से क्रिया होती है। |
|
5. हाइड्रॉक्साइड |
जल में अधिक विलेय और अधिक प्रबल क्षार है। |
जल में कम विलेय और कम क्षारीय है। |
|
6. कार्बोनेट |
जल में विलेय और गरम करने पर अपघटित नहीं होते हैं। |
जल में अविलेय और गरम करने पर ऑक्साइड और CO2 में अपघटित होते हैं। |
|
7. नाइट्रेटों को गरम करने |
नाइट्राइट तथा O2 में अपघटित हो जाते हैं। |
ऑक्साइड, NO2 तथा O2 में अपघटित हो जाते हैं। |
|
8. सल्फेट |
जल में विलेय हैं। |
जल में अविलेय हैं। |
विभिन्न प्रतियोगी परीक्षाओं में पूछे गये प्रश्न:
प्रश्न 1.
जलीय विलयन में आयनिक गतिशीलता का क्रम है:
(a) Rb+ > K+ > Cs+ > Na+
(b) Na+ > K+ > Rb+ > Cs+
(c) K+ > Na+ > Rb+ > Cs+
(d) Cs+ > Rb+ > K+ > Na+
उत्तर:
(d) Cs+ > Rb+ > K+ > Na+
प्रश्न 2.
क्षारीय धातुओं में सहसंयोजी प्रकृति के घटने का क्रम है:
(a) MCl > MI > MBr > MF
(b) MF > MCl > MBr > MI
(c) MF > MCl > MI > MBr
(d) MI > MBr > MCl > MF
उत्तर:
(d) MI > MBr > MCl > MF
प्रश्न 3.
निम्न में से किसको गर्म करने पर CO2 सर्वाधिक आसानी से उत्सर्जित होगी:
(a) K2CO3
(b) Na2CO
(c) MgCO3
(d) CaCO3
उत्तर:
(c) MgCO3

प्रश्न 4.
पोटेशियम का अयस्क है:
(a) कार्नेलाइट
(b) क्रायोलाइट
(c) बॉक्साइट
(d) डोलोमाइट
उत्तर:
(a) कार्नेलाइट
प्रश्न 5.
क्षार धातुओं में प्रबलतम अपचायक है:
(a) Li
(b) Na
(c) K
(d) Cs
उत्तर:
(a) Li
प्रश्न 6.
निम्नलिखित में से किसमें फिटकरी का उपयोग होता है:
(a) विस्फोटक बनाने में
(b) कपड़ों के विरंजन में
(c) जल मृदुकरण में
(d) सभी में
उत्तर:
(c) जल मृदुकरण में
प्रश्न 7.
सर्वाधिक स्थायी यौगिक है:
(a) LiF
(b) LiCl
(c) LiBr
(d) LiI
उत्तर:
(a) LiF
प्रश्न 8.
निम्नलिखित में से कौनसा हाइड्रॉक्साइड जल में अविलेय होता है?
(a) Mg (OH)2
(b) Be (OH)2
(c) Ba(OH)2
(d) Ca(OH)2
उत्तर:
(b) Be (OH)2
प्रश्न 9.
एक ठोस यौगिक X को गर्म करने पर CO2 गैस निकलती है तथा अवशेष में जल मिलाने पर यौगिक Y बनता है, Y के जलीय विलयन में आधिक्य में CO2 गैस प्रवाहित करने पर यौगिक Z का विलयन प्राप्त होता है तथा इसे गर्म करने पर पुनः यौगिक X बनता है तो यौगिक X है
(a) K2CO3
(b) CaCO3
(c) Ca(OH)2
(d) Na2CO3
उत्तर:
(b) CaCO3
प्रश्न 10.
क्षारीय धातुओं की विशेषताएँ हैं:
(a) ऊष्मा तथा विद्युत की अच्छी सुचालक होती है
(b) उच्च गलनांक
(c) निम्न ऑक्सीकरण विभव
(d) उच्च आयनन विभव
उत्तर:
(a) ऊष्मा तथा विद्युत की अच्छी सुचालक होती है
प्रश्न 11.
पदार्थों के संघटन के लिए सूची I का सूची II से सुमेल कीजि तथा लिस्ट के नीचे दिए गये कूट का प्रयोग करके सही उत्त चुनिये:
|
सूची I पदार्थ |
सूची II संघटन |
|
(A) प्लास्टर ऑफ पेरिस |
(i) CaSO4 . 2H2O |
|
(B) एप्सोमाइट |
(ii) CaSO4 12H2O |
|
(C) किसेराइट |
(iii) MgSO4 . 7H2O |
|
(D) जिप्सम |
(iv) MgSO4 . H2O |
उत्तर:
|
सूची I पदार्थ |
सूची II संघटन |
|
(A) प्लास्टर ऑफ पेरिस |
(i) CaSO4 . 2H2O |
|
(B) एप्सोमाइट |
(ii) CaSO4 12H2O |
|
(C) किसेराइट |
(iii) MgSO4 . 7H2O |
|
(D) जिप्सम |
(iv) MgSO4 . H2O |

प्रश्न 12.
भारत में शादी के अवसर पर आतिशबाजी का उपयोग होता है जहरी ज्वाला भी देती है। निम्न में से कौनसा मूलक उनमें उपस्थि हो सकता है:
(a) Na
(b) K
(c) Ba
(d) Ca
उत्तर:
(c) Ba
प्रश्न 13.
निम्नलिखित में से एप्सम लवण कौनसा है?
(a) CaSO4. H2O
(b) BaSO4.2H2O
(c) MgSO4 . 7H2O
(d) MgSO4.2H2O
उत्तर:
(c) MgSO4 . 7H2O
प्रश्न 14.
आयनिक त्रिज्याओं का सही क्रम कौनसा है?
(a) Mg2+ > Be2+ > Li+ > Na+
(b) Li+ > Na+ > Mg2+ > Be2+
(c) Na+ > Li+ > Mg+2 > Be2+
(d) Li+ > Be2+ > Na+ > Mg2+
उत्तर:
(c) Na+ > Li+ > Mg+2 > Be2+
प्रश्न 15.
निम्न में से कौन मैग्नीशियम का प्रमुख स्रोत है तथा एक द्विक लवण भी है:
(a) MgCO3
(b) Mg2P2O7
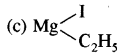
(d) KCl.MgCl2.6H2O
उत्तर:
(d) KCl.MgCl2.6H2O
प्रश्न 16.
पेड़-पौधों के हरे रंग के वर्णक क्लोराफिल में कौन-सा धातु तत्व पाया जाता है?
(a) Fe
(b) Mg
(c) Na
(d) Al
उत्तर:
(b) Mg
प्रश्न 17.
वह अयस्क जिसमें मैग्नीशियम व कैल्शियम दोनों धातुएँ हैं:
(a) मैग्नेसाइट
(b) डोलोमाइट
(c) कार्नेलाइट
(d) फॉस्फोराइट
उत्तर:
(b) डोलोमाइट
प्रश्न 18.
निम्नलिखित में से कौनसा कथन असत्य है?
(a) Li, N2 के साथ Li3N बनाता है।
(b) LiCl को आर्द्रता नियन्त्रण करने में उपयोग लिया जा सकता है।
(c) संगलित LiCl के विद्युत अपघटन से Li धातु बनाया जाता है।
(d) जलीय विलयन में Li+ की आयनिक गतिशीलता Na+ से ज्यादा होती है।
उत्तर:
(d) जलीय विलयन में Li+ की आयनिक गतिशीलता Na+ से ज्यादा होती है।
प्रश्न 19.
नाइट्रोलिम है:
(a) Ca(NO3)2
(b) Ca(CN)2
(c) CaCN2 + C
(d) CaCN2
उत्तर:
(c) CaCN2 + C
प्रश्न 20.
क्षारीय मृदा धातुओं के यौगिकों की चुम्बकीय प्रकृति निम्नांकित होती है:
(a) प्रतिचुम्बकीय
(b) अनुचुम्बकीय
(c) लौहचुम्बकीय
(d) प्रतिलौहचुम्बकीय
उत्तर:
(a) प्रतिचुम्बकीय

प्रश्न 21.
हवा के आधिक्य में Li, Na और K के दहन पर बनने वाली मुख्य ऑक्साइड क्रमश: हैं:
(a) Li2O, Na2O2 तथा K2O
(b) Li2O2, Na2O2 तथा KO2
(c) Li2O, Na2O2 तथा KO2
(d) Li2O, Na2O तथा KO2
उत्तर:
(c) Li2O, Na2O2 तथा KO2
